
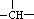 ,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)
,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)| A、4 | B、5 | C、6 | D、9 |
| 86-2 |
| 14 |
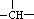 ,说明该烷烃只含有1个支链,其支链不可能为乙基,只能是甲基,该有机物可能的结构简式有2种:CH3CH(CH3)CH2CH2CH3、CH3CH2CH(CH3)CH2CH3,然后根据这两种有机物分子中含有的不同位置的H的数目判断其一氯代物种类.
,说明该烷烃只含有1个支链,其支链不可能为乙基,只能是甲基,该有机物可能的结构简式有2种:CH3CH(CH3)CH2CH2CH3、CH3CH2CH(CH3)CH2CH3,然后根据这两种有机物分子中含有的不同位置的H的数目判断其一氯代物种类.| 86-2 |
| 14 |
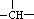 ,则该己烷分子中只能含有1个支链甲基,不会含有乙基,其主链含有5个C,满足条件的己烷的结构简式为:①CH3CH(CH3)CH2CH2CH3,②CH3CH2CH(CH3)CH2CH3,其中①分子中含有5种位置不同的H,即含有一氯代物的数目为5;②分子中含有4种位置不同的H,则其一氯代物有4种,所以该结构的烃的一氯取代物最多可能有:5+4=9种,
,则该己烷分子中只能含有1个支链甲基,不会含有乙基,其主链含有5个C,满足条件的己烷的结构简式为:①CH3CH(CH3)CH2CH2CH3,②CH3CH2CH(CH3)CH2CH3,其中①分子中含有5种位置不同的H,即含有一氯代物的数目为5;②分子中含有4种位置不同的H,则其一氯代物有4种,所以该结构的烃的一氯取代物最多可能有:5+4=9种,

科目:高中化学 来源: 题型:
| A、CH3(CH2)4CH3 |
| B、(CH3)2CHCH(CH3)2 |
| C、(C2H5)2CHCH3 |
| D、C2H5C(CH3)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、硫原子的原子结构示意图: | ||
B、NH4Cl的电子式: | ||
C、原子核内有10个中子的氧原子:
| ||
| D、乙烯的结构式为:CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(OH-) |
| c(H+) |
| A、该溶液中由水电离产生的c(H+)=1×10-8mol/L |
| B、0.01mol/LHA的溶液中c(H+)=1×10-4mol/L |
| C、1体积pH=3的HA与10体积pH=11的NaOH混合后溶液中c(OH-)+c(A-)═c(H+)+c(Na+) |
| D、浓度均为0.1 mol/L的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、C的氧化物对应的水化物一定为强酸,且只有氧化性 |
| B、三种元素对应的氢化物中B的氢化物稳定性最好 |
| C、原子半径大小关系为:B>A |
| D、C的单质常温下为无色无味的气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性强弱的顺序为:XO4一>Z2>B2>A3+ |
| B、Z2在①、③反应中为还原剂 |
| C、溶液中可发生:Z2+2A2+=2A3++2Z一 |
| D、X2十是XO4一的氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液氯能使干燥的有色布条褪色 |
| B、氯气与单质铁反应后,铁元素化合价变为+2价 |
| C、新制氯水呈黄绿色是因为其中存在氯气 |
| D、久置氯水遇AgNO3溶液不会产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
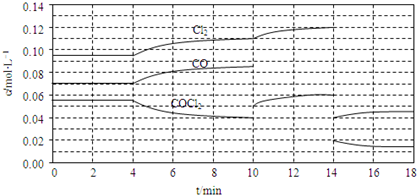
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com