
常温时,下列溶液的pH或微粒的物质的量浓度关系不正确的是 ( )
A.将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1 NaOH溶液等体积混合后,混合液pH大于7,则反应后的混合液:2c(OH一)+c(A一)=2c(H+)+c(HA)
B.某溶液中存在的离子有Cl-、OH-、NH4+、H+,则离子浓度不一定是
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:2c(R2-)+c(HR一)=c(Na+)
D.某物质的溶液中由水电离出的c(H+)=1×10-a mol•L-1,若a>7时,则该溶液的pH一定为14-a
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
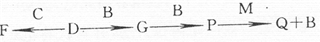
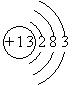

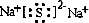
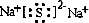


查看答案和解析>>
科目:高中化学 来源: 题型:
(08浙江省开化中学模拟)下列事实中,能证明NH3?H2O是弱电解质的是( )
A.常温时,稀氨水的导电性比稀NaOH溶液的导电性弱
B.常温时,等浓度等体积的氨水和盐酸混合,混合液pH小于7
C.1mol?L-1的氨水可以使酚酞试液变红色
D.液氨不导电
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年温州市适应性测试)下列说法正确的是( )
A.常温时,NaHCO3 溶液的pH 值比同浓度的CH3COONa 溶液小
B.常温时,pH=3的硫酸与pH=11的氨水等体积混合后,溶液呈酸性
C.把FeCl 和FeCl2溶液分别蒸干并灼烧最后都得到Fe203 固体
D.以酚酞作指示剂,用相同浓度的盐酸滴定等体积等浓度的NaOH溶液和氨水,消耗盐酸的体积相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com