
下列画有横线的反应物在反应中不能完全消耗的是( )
A.将含有少量CO2的CO通入足量Na2O2的试管中并不断用电火花引燃
B.向等物质的量的干冰和CaO的混合物中加几滴水
C.将1molCu置于含2molH2SO4的浓溶液中加热
D.在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2
C
【解析】
试题分析:A.将含有少量CO2的CO通入足量Na2O2的试管中并不断用电火花引燃,反应的总方程式是:CO+ Na2O2= Na2CO3,CO会被消耗,错误;B.向等物质的量的干冰和CaO的混合物中加几滴水,反应的总方程式是CO2+CaO=CaCO3;干冰会被消耗,错误;C.将1molCu置于含2molH2SO4的浓溶液中加热,反应的方程式是:Cu+2H2SO4(浓)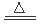 CuSO4+SO2↑+2H2O。Cu只能与浓硫酸反应,随着反应的进行,硫酸变稀,这时反应就不再发生,因此Cu不能完全反应,正确;D.在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2,发生反应:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO
CuSO4+SO2↑+2H2O。Cu只能与浓硫酸反应,随着反应的进行,硫酸变稀,这时反应就不再发生,因此Cu不能完全反应,正确;D.在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2,发生反应:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO 2HCl+ O2↑. Ca(ClO)2+2HCl=CaCl2+2HClO;所以Ca(ClO)2最终会完全发生反应,错误。
2HCl+ O2↑. Ca(ClO)2+2HCl=CaCl2+2HClO;所以Ca(ClO)2最终会完全发生反应,错误。
考点:考查在化学反应中物质能否完全反应的知识。


科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:选择题
下列有关实验装置进行的相应实验,能达到实验目的的是

图1 图2 图3 图4
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:填空题
(10分).查资料得:HNO2是一种弱酸且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。
试回答下列问题:
(1)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别 D. 用AgNO3和HNO3两种试剂来区别
(2)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的
Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(3) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
A.Cl2 B.Fe C.H2O2 D.HNO3
(4)某同学把酸性高锰酸钾溶液滴入NaNO2溶液中,观察到紫色褪去,同时生成NO3-和Mn2+,请写出反应的离子方程式:_____________________________________________。
(5)已知FeSO4在一定条件下可转变为高铁酸钾(K2FeO4),高铁酸钾是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是_______________________________________。
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
下列有关试验的做法不正确的是
A. 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
B.配置0.1000 mol·L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
C. 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
D.分液时,分液漏斗的顶塞应打开或使塞上凹槽与壁上小孔对准
查看答案和解析>>
科目:高中化学 来源:2015届江西五校高三第一次联考化学试卷(解析版) 题型:选择题
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如下图所示,下列说法中不正确的是( )

A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I- =2Fe2++I2
C.开始加入的K2Cr2O7为0.25 mol
D.K2Cr2O7可与FeSO4反应的物质的量为1:3。
查看答案和解析>>
科目:高中化学 来源:2015届江西五校高三第一次联考化学试卷(解析版) 题型:选择题
下列实验误差分析错误的是
A.用湿润的pH试纸测稀碱液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:填空题
(15分)某科研小组设计出利用工业废酸(稀H2SO4)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如下图所示。

已知:各离子开始沉淀及完全沉淀时的pH如下表所示。
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe2+ | 6.34 | 9.7 |
Fe3+ | 1.48 | 3.2 |
Zn2+ | 6.2 | 8.0 |
请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是 。
(2)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(3)物质A最好使用下列物质中的。
A.KMnO4B.空气C.HNO3D.NaClO
(4)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在范围之间。
(5)物质B可直接用作氮肥,则B的化学式是。
(6)除铁后得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂——K2FeO4,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.核内有8个中子的碳原子: B.甲烷分子的比例模型:
B.甲烷分子的比例模型:
C.羟基的电子式: D.氯离子的结构示意图:
D.氯离子的结构示意图:
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
A.等质量的O2比O3能量低,由O2变O3 为放热反应
B.等质量的O2比O3能量低,由O2变O3 为吸热反应
C.3O2(g)=2O3 (g) △H=285.0 kJ/mol
D.O3比O2稳定,由O2变O3 为吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com