
 电镀厂曾采用有氰电镀工艺,处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用图装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率.
电镀厂曾采用有氰电镀工艺,处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用图装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率.分析 (1)根据题意可知,甲中的反应为NaClO将CN-离子氧化成CNO-;乙中的反应为酸性条件下CNO-与NaClO反应生成N2、CO2和Cl2.根据氧化还原反应配平;
(2)饱和食盐水除去氯化氢气体;铜网用来除去氯气;碱石灰作用是吸收二氧化碳;
(3)根据碳原子守恒,计算出被处理的CN-的物质的量,再利用200mL(其中CN-的浓度0.05mol/L)求出CN-被处理的百分率;处理的百分率偏低,说明反应生成二氧化碳没有完全生成碳酸钙沉淀;根据找出的原因提出合理建议.
解答 解:(1)根据题意可知,甲中的反应为NaClO将CN-离子氧化成CNO-,NaClO具有强氧化性,被还原为Cl-,反应离子方程式为CN-+ClO-═CNO-+Cl-;乙中的反应为酸性条件下CNO-与NaClO反应生成N2、CO2和Cl2,反应离子方程式为2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O,
故答案为:CN-+ClO-═CNO-+Cl-;2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O;
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等,饱和食盐水能够除去氯化氢杂质;铜网能够和氯气反应从而除去氯气杂质;避免空气中的二氧化碳进入戊装置造成测定数据的干扰,用碱石灰吸收二氧化碳,
故答案为:除去HCl气体;去除Cl2;防止空气中CO2进入戊中影响测定准确度;
(3)200mL(其中CN-的浓度0.05mol/L)混合液中含有的CN-的物质的量是:0.2L×0.05mol/L=0.01mol,根据碳原子守恒,最多生成0.01mol二氧化碳,所以石灰水过量,生成的碳酸钙的物质的量是:0.0082mol,反应的CN-的物质的量是0.0082mol,CN-被处理的百分率是:$\frac{0.0082mol}{0.01mol}$×100%=82%;
该测得值与工业实际处理的百分率相比总是偏低,可能的原因有:①装置乙、丙、丁中可能滞留有CO2、②CO2产生丁速度较快未与戊中丁澄清石灰水充分反应、③Cl2、HCl在丙、丁中未吸收完全等;
能提高准确度的建议有:建议一:不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;建议二:乙中瓶塞改为三孔塞,增加丁那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多到与Ca(OH)2反应.建议三:将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等,
故答案为:82%;①装置乙、丙、丁中可能滞留有CO2,②CO2产生丁速度较快未与戊中丁澄清石灰水充分反应,③Cl2、HCl在丙、丁中未吸收完全(三点中任意答两点即可);
建议一:不将甲中溶液一次全部加入乙中,改为分次加入,控制CO2的产生速度;
建议二:乙中瓶塞改为三孔塞,增加丁那个孔中插入一根导管到液面以下,反应结束后缓缓通入除去CO2的空气,使装置中滞留的CO2尽可能多到与Ca(OH)2反应.
建议三:将戊中澄清石灰水改为浓度较大到NaOH溶液,反应结束后戊中加入足量CaCl2后测沉淀质量等(三点中任意答一点即可).
点评 本题考查了电镀后的废水中CN-离子的含量测定,该题是高考中的常见题型,属于中等难度的试题,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生规范严谨的实验设计、操作能力.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{{V}_{m}nb}{m{N}_{A}}$ | B. | $\frac{{V}_{m}mb}{n{N}_{A}}$ | C. | $\frac{{V}_{m}n{N}_{A}}{mb}$ | D. | $\frac{nb{N}_{A}}{{V}_{m}m}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含1molFeI2溶液中通入标准状况下22.4LCl22Fe2++2I-+2Cl2=2Fe3++I2+2Cl- | |
| B. | 在Na2S溶液中滴加少量FeCl3 2Fe3++S2-═2Fe2++S↓ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫原子的原子结构示意图: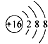 | |
| B. | NH4Cl的电子式: | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm为不同的核素,有不同的化学性质 | |
| D. | 在固态水中,水分子间以氢键结合成排列规整的晶体,在这种晶体中有空隙,造成体积膨胀,密度减小至低于水的密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 | |
| B. | 在纯锌与稀硫酸的反应混合物中滴入少量Cu(NO3)2溶液后生成H2的反应速率加快 | |
| C. | 各放一张质量相同的滤纸于天平的两托盘上,将NaOH固体放在左盘上称量 | |
| D. | 用如图所示装置吸收氨气可防倒吸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com