
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4 (C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | NH4Cl溶液 (FeCl3) | NaOH溶液 | 过滤 |
| C | 乙酸乙酯 (乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | C2H5OH (H2O) | 新制生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烯被高锰酸钾氧化生成二氧化碳;
B.二者都与氢氧化钠溶液反应;
C.乙酸与碳酸钠反应后与乙酸乙酯分层;
D.水与生石灰反应,可增大混合物的沸点差..
解答 解:A.乙烯被高锰酸钾氧化生成二氧化碳,引入新杂质,应加溴水利用洗气法除杂,故A错误;
B.二者都与氢氧化钠溶液反应,应加入氨水除杂,故B错误;
C.乙酸与碳酸钠反应后与乙酸乙酯分层,然后利用分液来分离,故C错误;
D.水与生石灰反应,可增大混合物的沸点差,可用蒸馏的方法分离,故D正确.
故选D.
点评 本题考查混合物分离提纯方法及选择,为高频考点,把握物质的性质及混合物分离方法为解答的关键,注重基础知识的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苯和液溴在FeBr3催化作用下生成溴苯 | |
| B. | 丙烯和氯气在一定条件下反应生成ClCH2CH=CH2的反应 | |
| C. | 乙烯使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯与HCl气体反应生成一氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子总数 | B. | 摩尔质量 | C. | 分子总数 | D. | 质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
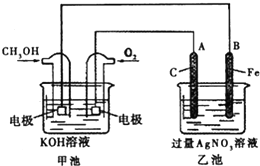 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中的信息,填写空格.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

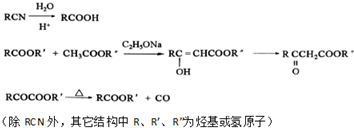
 ;E→F的反应类型取代反应
;E→F的反应类型取代反应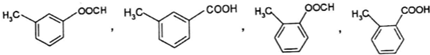 (其中一种).
(其中一种). 和苯环结构;
和苯环结构;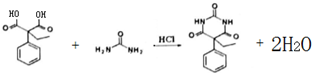 .
.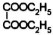 )的合成路线(用流程图表示;无机试剂任选).
)的合成路线(用流程图表示;无机试剂任选).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
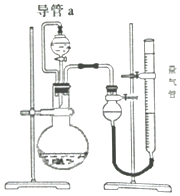 某兴趣小组的同学设计了如图装置进行试验探究,请回答下列问题:
某兴趣小组的同学设计了如图装置进行试验探究,请回答下列问题:| 序号 | 烧瓶中的物质 | 测得气体体积 |
| 实验1 | 20mL H2O2,足量MnO2 | V1 |
| 实验2 | 20mL H2O2,足量MnO2和稀硫酸 | V1<V2<2V1 |
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| Ⅰ | 1.0g | 10.00mL | 346.30mL |
| Ⅱ | 1.0g | 10.00mL | 335.50mL |
| Ⅲ | 1.0 g | 10.00mL | 346.00mL |
| Ⅳ | 1.0g | 10.00mL | 345.70mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com