
�������糧�ͷų������ĵ������NOx������������Ͷ�����̼���������ɻ�����Ⱦ����ȼú���������������������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ�
��1�����������ü������ԭNOx��
CH4��g����4NO2��g����4NO��g����CO2��g����2H2O��g�� ��H1����574 kJ��mol��1
CH4��g����4NO��g����2N2��g����CO2��g����2H2O��g�� ��H2����1160 kJ��mol��1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ ��
��2����̼����CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2��g����3H2��g�� CH3OH��g����H2O��g�� ��H3
��ȡ��ݵ������CO2��H2�Ļ�����壨���ʵ���֮�Ⱦ�Ϊ1��3�����ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״�����������գ�CH3OH�� �뷴Ӧ�¶�T�Ĺ�ϵ������ͼ��ʾ��
������CO2ת��Ϊ�״��ķ�Ӧ�ġ�H3__________0�����������������������
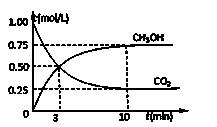
����һ���º����ܱ������г���1 mol CO2��3 mol H2������������Ӧ�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ���Իش�0~10 min�ڣ�������ƽ����Ӧ����Ϊ �����¶��£���Ӧ��ƽ�ⳣ����ֵΪ ����10 min������������ٳ���1 mol CO2��3 mol H2�����ٴδﵽƽ��ʱCH3OH��g����������� �������١����䣩��
��3������ij���������н���������������һ�����İ�����������Ӧ����������狀�����淋Ļ������Ϊ����Ʒ���ʡ��������£�a mol/L��(NH4)2SO4ˮ��Һ��pH=5��ԭ������Һ�д���ƽ��________________________(�����ӷ���ʽ��ʾ)���������ƽ���ƽ�ⳣ������ʽΪ________________________(�ú�����a�Ľ�Ϊ��ȷ����ѧ����ʽ��ʾ�����ػ�������������)��
����һ�����ʵ���Ũ�ȵ��������Һ�еμ�������NaOH��Һ��ʹ��Һ��pH=7������Һ��c(Na+) + c(H+)_____c(NO3-) + c(OH-)����д ������������������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
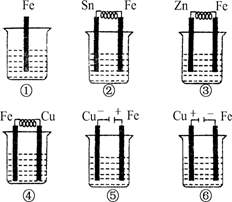
����ͼ��ʾ�����ձ���ʢ�к�ˮ����(������C)�����б���ʴ�ɿ쵽����˳��Ϊ�� ��
A���ڢ٢ۢܢݢ� B���ݢܢۢ٢ڢ�
C���ݢܢڢ٢ۢ� D���ݢۢڢܢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���� ��������
A��ˮ�����ӻ�KWֻ���¶��йأ�������ᡢ���һ����Ӱ��ˮ�ĵ���̶�
B��Ksp���������ܵ���ʵ����ʺ��¶��йأ�������Һ��������ӵ�Ũ���й�
C�������£���0.10 mol��L��1��NH3��H2O��Һ�м�������NH4C1���壬��ʹ��Һ��pH
��С��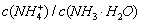 �ı�ֵ����
�ı�ֵ����
D�������£�CH3COOH��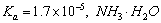 ��
��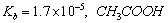 ��Һ�е�c (H+)��NH3��H2O�е�c(OH��)���
��Һ�е�c (H+)��NH3��H2O�е�c(OH��)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ��������ʵ����ʵ�������в���ȷ����(����)
A����50mL��ʽ�ζ���ȷ��ȡ25.00mL����KMnO4��Һ��������ƿ����
B�������£��ⶨŨ��Ϊ0.1 mol��L��1 NaClO��Һ��0.1 mol��L��1CH3COONa��Һ��pH���Ƚ�HClO��CH3COOH������ǿ��
C��ʵ���������Ȼ�������Һʱ�����Ȼ��������ܽ��������У�Ȼ��������ˮϡ�Ͳ�������������
D������1 mol��L��1��NaOH��Һʱ�����в��������������Ũ��ƫ�ͣ�����ʱ���ӿ̶��ߣ�����ƿ��ԭ����������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����(����)
A�������£���0.1 mol��L��1NH4HSO4��Һ�еμӵ����ʵ������ʵ�NaOH��Һ��c(Na��)=c(SO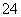 )>c(NH
)>c(NH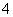 )>c(OH��)��c(H��)
)>c(OH��)��c(H��)
B��0.1 mol��L��1NaHCO3��Һ��c(Na��)��c(OH��)��c(HCO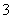 )��c(H��)
)��c(H��)
C��Na2CO3��Һ��c(OH��)��c(H��)��c(HCO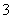 )��2c(H2CO3)
)��2c(H2CO3)
D��25��ʱ��pH��4.75��Ũ�Ⱦ�Ϊ0.1 mol��L��1��CH3COOH��CH3COONa�����Һ��c(CH3COO��)��c(OH��)<c(CH3COOH)��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��������ʵ�������ȷ����
A��Ư����Һ�ڿ�����ʧЧ��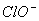 ��CO2��H2O=HClO��
��CO2��H2O=HClO��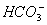
B����Ũ������MnO2��Ӧ��ȡ����������MnO2��2H����2Cl�� Mn2����Cl2����2H2O
Mn2����Cl2����2H2O
C����NaAlO2��Һ��ͨ�����CO2��Al(OH)3��AlO2����CO2��2H2O=Al(OH)3����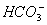
D����ǿ����Һ�д���������Fe(OH)3��Ӧ����Na2FeO4��3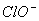 ��2Fe(OH)3=2
��2Fe(OH)3=2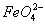 ��3
��3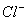 ��H2O��4H��
��H2O��4H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)��NaHSO4��Һ�У���μ���Ba(OH)2��Һ�������ԣ���д��������Ӧ�����ӷ���ʽ�� ��
(2)������������Һ�У������μ�Ba(OH)2��Һ����д���˲���Ӧ�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ˮ�����ؽ���Ǧ����Ⱦ���ⱸ�ܹ�ע��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2+��Pb(OH)+��Pb(OH)2��Pb(OH)3-��Pb(OH)42-������̬��Ũ�ȷ���������ҺpH�仯�Ĺ�ϵ��ͼ��ʾ��
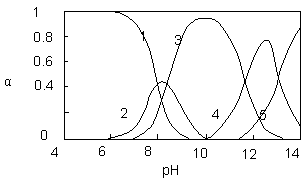
��1��ʾPb2+��2��ʾPb(OH)+��3��ʾPb(OH)2��4��ʾPb(OH)3-��5��ʾPb(OH)42-��
��Pb(NO3)2��Һ�У�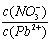 2 (�>������=������<��)��������Һ�е����Ȼ����Һ��
2 (�>������=������<��)��������Һ�е����Ȼ����Һ��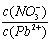 ���ӣ����ܵ�ԭ���� ��
���ӣ����ܵ�ԭ���� ��
����Pb(NO3)2��Һ�е�ϡNaOH��Һ��pH=8ʱ��Һ�д��ڵ�������(Na+����)��
��pH=9ʱ����Ҫ��Ӧ�����ӷ���ʽΪ ��
��ij�������Ʊ���һ��������Ǧ��������Чȥ��ˮ�еĺ���Ǧ��ʵ�������±���
 |
 ���� Pb2+ Ca2+ Fe3+ Mn2+ Cl-
���� Pb2+ Ca2+ Fe3+ Mn2+ Cl-
����ǰŨ��/(mg��L-1) 0.20130 29.8 0.120 0.087 51.9
������Ũ��/(mg��L-1) 0.004 22.6 0.040 0.053 49.8
 �ϱ��г�Pb2+�⣬����Ǧ�����������ӵ�ȥ��Ч����õ��� ��
�ϱ��г�Pb2+�⣬����Ǧ�����������ӵ�ȥ��Ч����õ��� ��
���������Ǧ��(��EH��ʾ)��Ǧ��������Ҫ�����ķ�ӦΪ��
2EH(s)+Pb2+ E2Pb(s)+2H+
E2Pb(s)+2H+
����Ǧ�������pH��ΧΪ (�����)��
A��4��5 B��6��7 C��9��2013 D��2013��12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�÷�̪��ʯ�0.1mol/L��ˮ���Ȼ�茶��塢0.1mol/L���ᡢ��ʯ�Һ�����ˮ��������
�����Լ������ü�ʵ�鷽��֤����ˮ�������ָ����ͨ��ʲô;��֤����ˮ������ģ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com