

| A. | 铜丝表面有气泡产生 | |
| B. | 铁钉上发生的反应为:Fe-3e-═Fe3+ | |
| C. | 一段时间后铁钉上出现红色物质 | |
| D. | 如果把铜丝换成镁条,会加快铁钉的溶解 |
分析 Cu、Fe和NaCl溶液构成原电池,发生吸氧腐蚀,Fe易失电子发生氧化反应而作负极、Cu作正极,正极上氧气得电子发生还原反应,据此分析解答.
解答 解:Cu、Fe和NaCl溶液构成原电池,发生吸氧腐蚀,Fe作负极、Cu作正极,正极上氧气得电子发生还原反应,
A.Cu丝表面电极反应式为O2+4e-+2H2O=4OH-,所以Cu丝表面没有气泡产生,故A错误;
B.Fe是负极,电极反应式为Fe-2e-=Fe2+,故B错误;
C.负极反应式为Fe-2e-=Fe2+、正极反应式为O2+4e-+2H2O=4OH-,Fe2+、OH-反应生成Fe(OH)2,Fe(OH)2不稳定,被空气氧化生成Fe(OH)3,Fe(OH)3失水生成带结晶水的氧化铁,即铁锈,所以看到的现象是一段时间后铁钉上出现红色物质,故C正确;
D.如果把铜丝换成镁条,Mg易失电子作负极、Fe作正极而被保护,故D错误;
故选C.
点评 本题考查原电池原理,侧重考查电化学知识,明确原电池正负极的判断、电极反应即可解答,易错选项是A,注意铁发生析氢腐蚀与吸氧腐蚀区别,题目难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:选择题
| A. | Al:1s22s22p63s2 | B. | O2-:1s22s22p6 | ||
| C. | Na+:1s22s22p63s1 | D. | Si:1s22s22p63s23p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
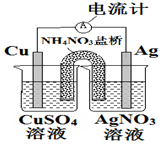
| A. | 盐桥中的NH4+离子向左侧烧杯移动 | |
| B. | 铜电极上发生的反应为Cu-2e-═Cu2+ | |
| C. | 外电路中的电子是从银电极流向铜电极 | |
| D. | 该装置能将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )
如图是部分短周期元素的原子序数与其某种常 见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中不正确的有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| t/min | 0 | 20 | 40 | 60 | 80 | 120 | |
| 第一次试验 | x(HI) | 1 | 0.90 | 0.85 | 0.815 | 0.795 | 0.784 |
| 第二次试验 | x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 常温常压下,44g CO2含有的原子数为3NA | |
| C. | 常温常压下,11.2L氧气所含的原子数为NA | |
| D. | 标准状况下,11.2L H2O 含有的分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com