
有两试管分别装有Na2CO3和NaHCO3溶液,下列操作或判断正确的是
| 方案 | 操作 | 判断 |
| A | 分别加入澄清石灰水 | 产生沉淀者为Na2CO3 |
| B | 分别加入等浓度的稀盐酸 | 反应较剧烈者为Na2CO3 |
| C | 分别加入CaCl2溶液 | 产生沉淀者为Na2CO3 |
| D | 逐渐加入等浓度的盐酸 | 立即产生气泡者为Na2CO3 |
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
下列说法或表示方法中正确的是 ( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)→C(石墨)ΔH= -1.9KJ/mol 可知,金刚石比石墨稳定
C.在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气的燃烧热化学方程式为:2H2(g)+O2(g)=2H2O(l) ΔH= - 285.8KJ/mol
D. 稀硫酸与稀NaOH溶液反应的中和热为ΔH= -57.3 kJ /mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)====CO2(g)+2H2O(l) ΔH=+725.8 kJ·mol-1
O2(g)====CO2(g)+2H2O(l) ΔH=+725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1
C.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)====2CO2(g)+4H2O(l) ΔH=+1 452 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是
A.非金属单质燃烧时火焰均为无色
B.所有金属及其化合物灼烧时火焰均有颜色
C.焰色反应均应透过蓝色钴玻璃观察
D.NaCl与Na2CO3灼烧时火焰颜色相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于纸色谱法分离Fe3+和Cu2+操作正确的是( )
A.裁滤纸应垂直纤维方向裁开
B.点样时,斑点尽量小,且再点时必须在同一位置
C.展开时,用流动相溶剂刚好淹过色斑进行展开
D.当流动相溶剂上升至滤纸上沿时,取出晾干观察
查看答案和解析>>
科目:高中化学 来源: 题型:
用一种只有水分子能自由通过而直径较大的溶质分子不能通过的隔膜把水槽隔离成大小完全相同的甲、乙两室,甲室中装入淀粉溶液,乙室中装入蒸馏水(如图)。此时甲、乙两室中的水分子均可自由地通过隔膜而相互扩散,已知这种扩散速度与单位体积内溶质的微粒数成反比,而与液体的压强成正比。
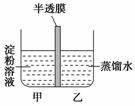
根据以上叙述回答下列问题:
(1)若甲、乙两室中装入液体的体积相同,对于实验开始阶段的描述正确的是________。
A.水分子从甲室向乙室的扩散速度大于乙室向甲室的扩散速度
B.水分子从乙室向甲室的扩散速度大于甲室向乙室的扩散速度
C.两室中水分子的相互扩散速度相等
D.两室中水分子的扩散速度将越来越小
(2)相同温度下,甲室装入质量分数为1%的尿素[CO(NH2)2]水溶液,乙室装入等体积的质量分数为a%的葡萄糖(C6H12O6)溶液,若两溶液的密度近似看成1 g·cm-3,且水分子相互扩散的速度也相等,则a的近似值是________。
A.1 B.2
C.3 D.4
查看答案和解析>>
科目:高中化学 来源: 题型:
现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验。实验过程和记录如下图所示(无关物质已经略去):
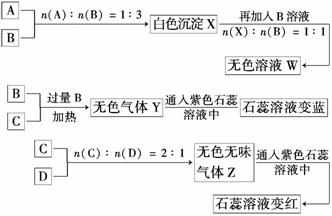
请回答:
(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为______、______。
(2)D溶液pH______7(填“大于”、“小于”或“等于”),原因是(用离子方程式表示)________________________________________________________________________。
(3)等物质的量浓度的A、B、C、D溶液,pH由大到小的顺序是______________________________________ __________________________________
__________________________________
(用化学式表示)。
(4)等物质的量浓度的C溶液与NH4Cl溶液相比较,c(NH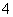 ):前者________后者(填“<”、“>”或“=”)。
):前者________后者(填“<”、“>”或“=”)。
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是____________________________________ ____________________________________
____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下进行性质比较的实验设计,不合理的是
A.比较镁、铝金属性:镁、铝(除氧化膜)分别放入4 mol·L-1NaOH溶液中
B.比较氯、溴非金属性:氯气通入溴化钠溶液中
C.比较Cu、Fe2+的还原性:Cu加入FeCl3溶液中
D.比较高锰酸钾、氯气的氧化性:高锰酸钾中加入浓盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com