
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:选择题
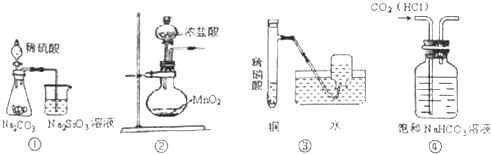
| A. | 图①可证明酸性强弱:H2SO4>H2CO3>H2SiO3 | |
| B. | 图②可用于实验室制备少量氯气 | |
| C. | 图③可用于实验室制备少量NO气体 | |
| D. | 图④可除去CO2中少量HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可使蛋白质变性,故可浸制标本 | |
| B. | 海水提取溴、煤的液化、纯碱去油污都发生了化学变化 | |
| C. | 钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高 | |
| D. | Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚类和醇类具有相同的官能团,因而具有相同的化学性质 | |
| B. | 含有羟基的化合物属于醇类 | |
| C. | 羟基跟链烃基直接相连的化合物属于醇类 | |
| D. | 分子内含有苯环和羟基的化合物都属于酚类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,若有6mol电子发生转移,则有2mol K2FeO4被氧化 | |
| B. | 放电时,正极反应为:FeO42-+4H2O+3e-═Fe(OH)3+5OH- | |
| C. | 充电时,电池的负极与外接电源的正极相连 | |
| D. | 充电时,阴极附近溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2 | B. | NaHCO3 | C. | HCl | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯和乙烯性质相似,都能发生加成反应 | |
| B. | 纤维素、橡胶和光导纤维都属于有机高分子化合物 | |
| C. | 乙烯和乙醇都可发生加成反应 | |
| D. | 等量的CH4和Cl2在光照下反应不能生成纯净的CH3Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素和蛋白质均属于高分子化合物 | |
| B. | 用漂白粉漂白时,向水溶液中加几滴白醋,会增强漂白效果 | |
| C. | 利用乙醇的还原性以及Cr3+、Cr2O7-的颜色差异来检验酒后驾车 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
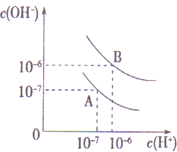 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com