
 CH3CH2OH(l) + CH3COOH(l) ;△H
CH3CH2OH(l) + CH3COOH(l) ;△H
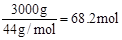 ,因为乙醛的去除率为60%,则生成乙醇68.2mol× 60%=40.9mol,质量为40.9mol×46g/mol=1882g≈1.9kg。
,因为乙醛的去除率为60%,则生成乙醇68.2mol× 60%=40.9mol,质量为40.9mol×46g/mol=1882g≈1.9kg。

科目:高中化学 来源:不详 题型:单选题
| A.(c-a-b)kJ | B.(a+b-c)kJ |
| C.(2c-a-b)kJ | D.(2c-a-b)/2kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4Q | B.5Q | C.8Q | D.16Q |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·
 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·
 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·
| A.a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1+Q2+Q3 |
| B.0.5Q1-0.5Q2+1.5Q3 |
| C.0.5(Q1+Q2+Q3) |
| D.0.5Q1-1.5Q2+0.5Q3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.有NA的个电子转移时,该反应放出1300KJ的能量 |
| B.有NA个水分子生成且为液体时,吸收1300KJ的能量 |
| C.有2NA个碳氧共用电子对生成时,放出1300KJ的能量 |
| D.有8NA个碳氧共用电子生成时,放出1300KJ的能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
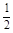 O2(g) =H2O(l) △H2=–285.8 kJ/mol
O2(g) =H2O(l) △H2=–285.8 kJ/mol| A.△H=244.1kJ/mol | B.△H=-488.3kJ/mol |
| C.△H=-996.6kJ/mol | D.△H=996.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
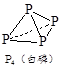
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com