
【题目】
A. Fe、 Mn、 Zn、 Mg B. Zn、 Cu、 Mn、 Ca
C. Zn、 Cu、 B、 Mn D. Mg、 Mn、 Cu、Mo
科目:高中化学 来源: 题型:
【题目】磷是生物体中不可缺少的元素之一它能形成多种化合物。
(1)磷元素位于周期表的______区,基态磷原子价层电子排布图_______。
(2)第三周期中第一电离能位于铝元素和磷元素之间的元素有________种。
(3)白磷(P4)分子是正四面体结构,磷原子杂化方式为______,3.1g白磷中σ键的数目为___。P4易溶于二硫化碳,难溶于水,原因是___________。
(4)磷酸与Fe3+可形成H3[FePO4)2],基态Fe3+的核外电子排布式为______,Fe、P、O电负性由大到小的顺序是____________。
(5)磷化硼是一种超硬耐磨涂层材料,下图为其晶胞结构,阿伏伽德罗常数为NA,磷化硼晶体的密度为ρg/cm3,B与P最近距离为______cm(列出计算式即可),估测该晶体的熔点_______(填“高于”或“低于”)金刚石。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰干电池在放电时电池总反应方程式为Zn+2MnO2+2NH![]() ===Zn2++Mn2O3+2NH3↑+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
===Zn2++Mn2O3+2NH3↑+H2O。在此电池放电时,正极(碳棒)上发生反应的物质是( )
A. 锌 B. MnO2和NH![]() C. 碳 D. Zn2+和NH3
C. 碳 D. Zn2+和NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(5分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。

回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( ) 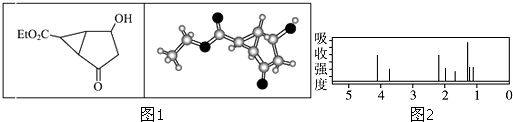
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香化合物
C.键线式中的Et代表的基团为﹣CH3
D.该有机物在一定条件下能够发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是锌片和铜片在稀硫酸中所组成的原电池装置,c、d为两个电极。下列有关的判断不正确的是

A. 电池工作的过程中,d电极上产生气泡
B. 电池工作时,溶液中SO42-向d移动
C. c为负极,发生氧化反应
D. 电池工作的过程中,溶液中SO42-浓度基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素。下列判断正确的是

A. 甲一定是金属元素
B. 气态氢化物的稳定性:庚>己>戊
C. 乙、丙、丁的最高价氧化物水化物可以以相互反应
D. 庚的最高价氧化物水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)X的原子结构示意图为 ______________。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):______> ;比较g、h的最高价氧化物对应水化物的酸性强弱: >_______。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com