
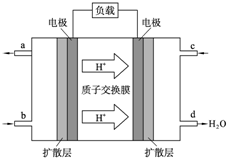
 人们应用原电池原理制作了多种电池以满足不同的需要.电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题:
人们应用原电池原理制作了多种电池以满足不同的需要.电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染.请根据题中提供的信息,回答下列问题:分析 (1)①负极上失电子发生氧化反应;
②原电池放电时,电解质溶液中阳离子向正极移动;
③根据Na2Mn5O10和转移电子之间的关系式计算.
(2)①根据氢离子移动方向知,右侧电极为正极,左侧电极为负极,负极上通入燃料;
②负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应;
③根据甲醇和转移电子之间的关系式计算;
(3)电池放电时正极的Ag2O2 转化为Ag,负极的Zn转化为K2Zn(OH)4,反应还应有KOH参加,依据转化写出电池反应.
解答 解:(1)①根据电池总反应:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,可判断出Ag应为原电池的负极,负极发生反应的电极方程式为:Ag+Cl--e-=AgCl,
故答案为:Ag+Cl--e-=AgCl;
②在原电池中阴离子向负极移动,阳离子向正极移动,所以钠离子向正极移动,故答案为:正;
③根据方程式中5MnO2生成1Na2Mn5O10,化合价共降低了2价,所以每生成1molNa2Mn5O10转移2mol电子,则外电路每通过4mol电子时,生成Na2Mn5O10的物质的量是2mol,故答案为:2mol;
(2)①据氢离子移动方向知,右侧电极为正极,左侧电极为负极,负极上通入燃料甲醇,故答案为:CH3OH;
②正极上氧气得电子和氢离子反应生成水,电极反应式为:3O2+12H++12e-=6H2O,负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为CH3OH-6e-+H2O=CO2+6H+,故答案为:CH3OH-6e-+H2O=CO2+6H+;
③根据2CH3OH-12e-+2H2O=2CO2+12H+知,甲醇和转移电子之间的关系式得,当6.4g甲醇完全反应生成CO2时,转移电子的物质的量=$\frac{6.4g}{32g/mol}$=1.2mol,则转移电子个数为1.2NA,故答案为:1.2;
(3)电池放电时正极的Ag2O2 转化为Ag,负极的Zn转化为K2Zn(OH)4,正极电极反应式为Ag2O2+4e-+2H2O═2Ag+4OH-,负极电极反应式为2Zn-4e-+8OH-═2Zn(OH)42-,反应还应有KOH参加,反应的总方程式为:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag,故答案为:Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag.
点评 本题考查原电池的电极反应和离子的定向移动以及电化学的简单计算,做题时要注意总电池反应式的判断利用,运用两极上的反应特点做题,分析Mn元素的化合价变化是该题的难点.


科目:高中化学 来源: 题型:选择题
| A. | 原电池中阴离子向正极移动 | |
| B. | 原电池是将电能转化为化学能的装置 | |
| C. | 原电池中电子流出的极为负极,发生氧化反应 | |
| D. | 原电池正极上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只要是在加热条件下进行的反应一定是吸热反应 | |
| B. | 一种能量形式可以转化为另外的能量,所以任何反应都可以把化学能转化为电能 | |
| C. | 中和反应和燃烧是放热反应,Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 只要反应物的总能量高于生成物的总能量,在任何条件下该反应就能够发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
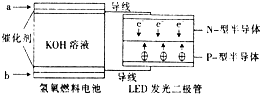 LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )
LED产品的使用为城市增添色彩.图是氢氧燃料电池驱动LED发光的一种装置示意图.下列有关叙述正确的是( )| A. | P-型半导体连接的是电池负极 | |
| B. | b处为电池正极,发生了还原反应 | |
| C. | a处通入氢气,发生还原反应 | |
| D. | 该装置中只涉及两种形式的能量转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
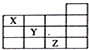
| A. | X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐 | |
| B. | 等物质的量浓度的X、Y、Z的气态氢化物的水溶液的pH:X>Y>Z | |
| C. | Z的单质常温下是液体,可与铁粉反应 | |
| D. | Z的原子序数比Y大9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com