
【题目】下列关于SiO2的说法,正确的是( )
A. SiO2是制造光导纤维的重要材料
B. SiO2溶于水生成硅酸
C. SiO2对应水化物的酸性比碳酸强
D. SiO2是两性氧化物
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列问题(答题时用具体元素符号表示). 
(1)用数字标注的元素中原子半径最小的是 , 半径最大的是 , 化学性质最稳定的是 , 非金属性最强的是 , 最高价氧化物对应的水化物酸性最强的是 .
(2)③最高价氧化物的结构式 , ⑦单质在⑤单质中燃烧生成物的电子式
(3)工业制取单质⑦的化学方程式 , 实验室制取单质⑨的化学方程式 , 单质⑧与单质⑦的最高价氧化物对应的水化物的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO ![]() 、SO
、SO ![]() 、Cl﹣、CO
、Cl﹣、CO ![]() 的某一种(1)若将四种盐分别溶于中水中,只有C盐溶液显蓝色.(2)若向四种溶液中分别加盐酸,B盐溶液中沉淀生成,D盐溶液中有无色无味的气体生成.根据以上事实,可推断:
的某一种(1)若将四种盐分别溶于中水中,只有C盐溶液显蓝色.(2)若向四种溶液中分别加盐酸,B盐溶液中沉淀生成,D盐溶液中有无色无味的气体生成.根据以上事实,可推断:
(1)A、B、C、D的化学式分别为:A、B、C、D、
(2)分别写出下列反应的离子方程式:A+DD与盐酸: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PVC是聚氯乙烯的英文缩写,为保证PVC塑料制品的性能,通常需要加入多种有机助剂。下列选项中的事实均能支持“PVC保鲜膜对人体健康带来危害”假设的是( )
①PVC塑料属于高分子材料
②使用的有机助剂有毒
③含氯的化合物不一定有毒
④在高温下会分解出有害物质
A.①②
B.③④
C.②④
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO47H2O)是治疗缺铁性贫血的特效药.某化学兴趣小组对绿矾进行了如下的探究: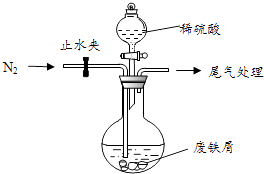
(1)【制备产品】
该小组由废铁屑(含少量氧化铜、氧化铁等杂质),用如图所示装置制备FeSO47H2O晶体,步骤如下:
①预处理:先将废铁屑加入到饱和Na2CO3溶液中洗涤,目的是 , 然后将废铁屑用水洗涤2~3遍.
②将洗涤后的废铁屑加入到圆底烧瓶中,并持续通入N2 , N2的作用是 .
③再加入足量稀硫酸,控制温度50℃~80℃之间,充分反应后,圆底烧瓶中剩余的固体为 .
④获取产品:先向步骤(3)中反应后的混合物中加入少许蒸馏水,趁热过滤, , . 滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干,密闭保存.
(2)【测定FeSO47H2O含量】
①称取上述样品10.0g,溶于适量的稀硫酸中,配成100mL溶液,需要的仪器除天平、胶头滴管、烧杯、量筒外,还需要的仪器有(填仪器名称)、 . 胶头滴管,250ml容量瓶…
②准确量取25mL该液体于锥形瓶中,用0.1000mol/L KMnO4标准溶液滴定,则滴定终点的判断方法是 .
③用同样的方法滴定3次,平均消耗10.00mL标准液,该样品中FeSO47H2O的质量分数为 . (已知Mr(FeSO47H2O)=278)
④若测量结果偏小,则可能是在定容时(填“俯视”或“仰视”)读数.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子浓度关系正确的是( )
A.pH=1的NaHSO4溶液:c(H+)=c(SO ![]() )+c(OH﹣)
)+c(OH﹣)
B.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl﹣)=c(I﹣)
C.CO2的水溶液:c(H+)>c(HCO ![]() )=2c(CO
)=2c(CO ![]() )
)
D.含等物质的量NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O ![]() )+c(C2O
)+c(C2O ![]() )+c(H2C2O4)]
)+c(H2C2O4)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铂电极电解某金属的硫酸盐(XSO4)溶液,当阳极上收集到1.12L气体(标准状况,忽略气体溶解)时,阴极质量增加6.4g,下列判断不正确的是( )
A. 电路中有0.1mol电子通过
B. 该金属是Cu
C. 电解后溶液的pH降低
D. 向电解后的溶液中加入0.1molCuO可使溶液恢复电解前的状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:【实验一】焦亚硫酸钠的制取
采用如图1装置(实验前已除尽装置内的空气)制取Na2S2O5 . 装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O5 . 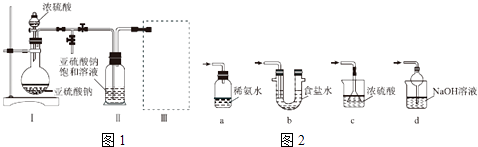
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为(填序号).
(4)【实验二】焦亚硫酸钠的性质:Na2S2O5溶于水即生成NaHSO3 . 证明NaHSO3溶液中HSO ![]() 的电离程度大于水解程度,可采用的实验方法是(填序号).
的电离程度大于水解程度,可采用的实验方法是(填序号).
a.测定溶液的pH b.加入Ba(OH)2溶液
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检测Na2S2O5晶体在空气中已被氧化的实验方案是
(6)【实验三】葡萄酒中抗氧化剂残留量的测定葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:![]()
(已知:滴定时反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为gL﹣1 .
②在上述实验过程中,若有部分HI被空气氧化,则测定结果(填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是_________________________。
(2)烧杯间填满碎纸条的作用是________________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值___________(填“偏大、偏小、无影响”)
(4)如果用50mL0.50mol/L硝酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_________________(填“相等、不相等”),所求中和热__________(填“相等、不相等”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com