
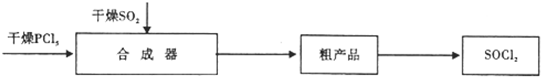
| 实验步骤 | 预期现象和结论 |
| 步骤1取少量吸收液于试管中滴加3moL.L-1H2SO4,至溶液呈酸性,然后将所得溶液分置于A、B试管中. | 无明显现象 |
| 步骤2:在A试管中滴加紫色石蕊试液 | 若先变红后褪色,证明有ClO-,否则无 |
| 步骤3:在B试管中滴加0.01mol•L-1KMnO4溶液 | 若紫红色褪去,证明有SO32-,否则无 |
分析 (1)根据二氧化硫的性质分析;
(2)分离沸点不同的混合体系用分馏(或蒸馏);
(3)合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0,需要耐高温、耐氧化、耐腐蚀的材料;
(4)已知SOCl2与H2O发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,说明生HCl气体和二氧化硫气体,据此书写;
(5)负极发生发生氧化反应结合总方程书写;
(6)加入硫酸至酸性,若存在SO32-、ClO-,分别生成了H2SO3和HClO;因为HClO具有酸性和漂白性,选择紫色石蕊试液,证明有ClO-的存在;H2SO3具有还原性,选择具有强氧化性高锰酸钾溶液,证明SO32-的存在.
解答 解:(1)二氧化硫为酸性氧化物,故不能用碱性干燥剂,可用浓硫酸或硅胶干燥;
故答案为:AD;
(2)亚硫酰氯(SOCl2)是一种液态化合物,沸点770C,粗产品中混有POCl3,沸点为105.3℃,分离沸点不同的混合体系用分馏(或蒸馏);
故答案为:分馏(或蒸馏);
(3)合成器中发生的反应为:PCl5(熔融)+SO2$\frac{\underline{\;一定温度\;}}{\;}$SOCl2+POCl3△H<0,需要耐高温、耐氧化、耐腐蚀的材料如工程陶瓷或耐高温陶瓷;
故答案为:耐高温、耐氧化、耐腐蚀(工程陶瓷或耐高温陶瓷);
(4)SOCl2与H2O发生剧烈反应,有白雾形成并逸出有剌激性气味的气体,说明生HCl气体和二氧化硫气体,则反应为:SOCl2+H2O=SO2↑+HCl↑;
故答案为:SOCl2+H2O=SO2↑+HCl↑;
(5)电池的总反应可表示为:Li+SOCl2═4LiCl+S+SO2,负极发生氧化反应,则负极为Li反应生成锂离子,电极反应式为:Li-e-=Li+;
故答案为:Li-e-=Li+;
(6)因为吸收液呈碱性,先取少量吸收液于试管中,滴加3moL-L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中先加入硫酸的试管,若存在SO32-、ClO-,分别生成了H2SO3和HClO;
在A试管中滴加紫色石蕊试液,若先变红后褪色,证明有ClO-,否则无;
在B试管中滴加0.01mol•L-1KMnO4溶液,若紫红色褪去,证明有SO32-,否则无;
故答案为: .
.
点评 本题考查性质实验方案设计,侧重考查学生知识综合应用、根据实验目的及物质的性质进行实验方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1molNH5中含有5NA个N-H键 | |
| B. | NH5中既含有共价键,又含有离子键,是离子化合物 | |
| C. | NH5的熔、沸点高于NH3 | |
| D. | NH5固体投入少量水中可产生两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性:Cl>Br | B. | 酸性:H2SO3>H2CO3 | ||
| C. | 碱性:KOH>NaOH | D. | 热稳定性:NH3>PH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 原子结构或性质 |
| A | 其形成的一种同位素元素在考古中可推测化石的年代 |
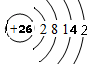
| B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
| C | 地壳中含量最多的元素 |
| D | D原子的最外层电子数与其电子层数相同,是地壳中含量最多的金属元素 |
| E | 其单质主要存在于火山口附近 |
| F | 生活中常见的金属,它的某种氧化物均有磁性 |
| G | G原子与D原子同周期,且原子半径是同周期元素中最大的 |
 ;
; ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯能使溴水褪色是因为苯与溴水发生了化学反应 | |
| B. | 欲从碘的苯溶液中分离出碘,通常采用萃取法 | |
| C. | 苯和不溶于水且密度比水大的四氯化碳都是无色液体,用试管和水就可以区别它们 | |
| D. | 因为苯通常是无色液体,所以在0℃的环境中可以直接将苯从试剂瓶倒人试管中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{14}$ mol•L-1 | B. | $\frac{4}{5}$ mol•L-1 | C. | $\frac{1}{28}$ mol•L-1 | D. | $\frac{1}{42}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L该溶液中含KNO3101g | |
| B. | 100 mL该溶液中含KNO3 0.01mol | |
| C. | 从1L该溶液中取出500 mL后,剩余溶液的浓度为0.05 mol/L | |
| D. | 1L水中溶解0.1 mol KNO3,即可配得0.1 mol/L KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
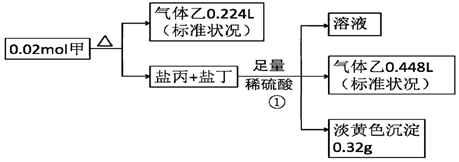
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com