
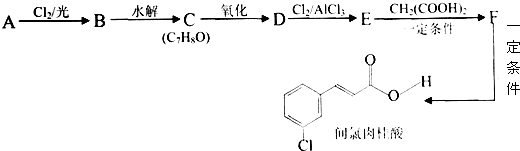
| 一定条件 |
| 一定条件 |
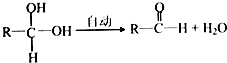
| Cl2/光 |
| 水解 |
 ,A为
,A为 ,B为
,B为 ,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为
,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为 ,E为
,E为 ,由信息I可知F为
,由信息I可知F为 ,据此解答.
,据此解答. ,A为
,A为 ,B为
,B为 ,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为
,C发生氧化反应生成D,而与氯气发生取代反应生成E,结合反应得到I,可知E中含有-CHO,由间氯肉桂酸的结构可知,Cl处于-CHO的间位,故D为 ,E为
,E为 ,由信息I可知F为
,由信息I可知F为 ,
, ,名称为甲苯,故答案为:甲苯;
,名称为甲苯,故答案为:甲苯; ,属于芳香醇,故选:C;
,属于芳香醇,故选:C; +Cl2
+Cl2| 光照 |
 +HCl;
+HCl; 在浓H2SO4存在下与冰醋酸共热发生酯化反应,该反应方程式为:
在浓H2SO4存在下与冰醋酸共热发生酯化反应,该反应方程式为: +CH3COOH
+CH3COOH| 浓硫酸 |
| △ |
 +H2O,
+H2O, +Cl2
+Cl2| 光照 |
 +HCl;
+HCl; +CH3COOH
+CH3COOH| 浓硫酸 |
| △ |
 +H2O;
+H2O;| Cl2/光 |
| 水解 |
 ,若G的一种同分异构体的核磁共振氢谱中只出现三个峰,且峰面积比为1:1:1,则含有侧链为-Cl、-CH2Cl且处于对位,则该同分异构体的结构简式为:
,若G的一种同分异构体的核磁共振氢谱中只出现三个峰,且峰面积比为1:1:1,则含有侧链为-Cl、-CH2Cl且处于对位,则该同分异构体的结构简式为: ,故答案为:
,故答案为: ;
; ,分子式为C10H7O4Cl,可以改写为C8H6.2CO2.HCl,间氯肉桂酸的分子式为C9H7O2Cl,可以改写为C8H6.CO2.HCl,1molF与1mol间氯肉桂酸的耗氧量均为(8+
,分子式为C10H7O4Cl,可以改写为C8H6.2CO2.HCl,间氯肉桂酸的分子式为C9H7O2Cl,可以改写为C8H6.CO2.HCl,1molF与1mol间氯肉桂酸的耗氧量均为(8+| 6 |
| 4 |


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
| A、N2H2 |
| B、N2H4 |
| C、NH2 |
| D、N2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32克O2所含的原子数目为2NA |
| B、0.5L 0.2mol/L的NaCl(aq)中含有的Na+数是0.1NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、0.5NA个氯气分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烧菜用过的铁锅,经放置常出现红棕色斑迹 |
| B、用煤气灶燃烧沼气主要成分为甲烷(CH4中C为+4价)为炒菜提供热量 |
| C、铜质炊具长久不用生铜锈 |
| D、灶具大理石板使用醋腐蚀变的不光滑 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在恒容密闭容器中进行的反应:2CO2(g)+6H2(g)?C2H5OH(g)+3H2O(g)△H.在某压强下起始时按不同氢碳[
在恒容密闭容器中进行的反应:2CO2(g)+6H2(g)?C2H5OH(g)+3H2O(g)△H.在某压强下起始时按不同氢碳[| n(H2) |
| n(CO2) |
| A、该反应:△H>0 |
| B、氢碳比:①<②<③ |
| C、其它条件不变的情况下,缩小容器的体积CO2的转化率降低 |
| D、若起始CO2浓度为2mol?L-1、H2为4mol?L-1,在图中曲线③氢碳比条件下进行,则400K时该反应的平衡常数数值约为1.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、充入一定量Z,X的体积分数增大 |
| B、增大压强,Z的浓度不变 |
| C、减小压强,Y的体积分数变大 |
| D、充入一定量X,平衡正向移动,X的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的最外层电子数是次外层电子数的2倍 |
| Y | Y的单质为黄色晶体,是制黑火药的原料之一 |
| Z | Z和Y同周期,原子半径:Y>Z |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com