
| A�� | ��ԭ�ӵ��������5�����ӣ����⻯�ﺬ�м��Լ� | |
| B�� | ����Ԫ���б��ķǽ�������ǿ��������������Ӧ�ĺ�����������ǿ | |
| C�� | ��Ԫ�ص��������Ӧ��ˮ��������Ԫ������������Ӧˮ������ȫ��Ӧ�γɵ��ε���Һ������ | |
| D�� | �ҡ�����Ԫ���γɵ��⻯���ȶ��Ա���ǿ���� |
���� ���мס��ҡ����������ֶ�����Ԫ�أ�ԭ�ӵĺ�����Ӳ�����������=��=2�ף���״��ڵ�һ���ڣ��ҡ������ڵڶ����ڣ������ڵ������ڣ��ʼ�ΪHԪ�أ���Ԫ�ص���Ҫ���ϼۣ��������+�����=2�����Ҵ���VA�壬����ΪNԪ�أ�ԭ�ӵ���������������+��=��+��=8���������������Ϊ8-1=7��������������Ϊ8-5=3���ʱ�ΪFԪ�أ���ΪAl���ݴ˽��
��� �⣺���мס��ҡ����������ֶ�����Ԫ�أ�ԭ�ӵĺ�����Ӳ�����������=��=2�ף���״��ڵ�һ���ڣ��ҡ������ڵڶ����ڣ������ڵ������ڣ��ʼ�ΪHԪ�أ���Ԫ�ص���Ҫ���ϼۣ��������+�����=2�����Ҵ���VA�壬����ΪNԪ�أ�ԭ�ӵ���������������+��=��+��=8���������������Ϊ8-1=7��������������Ϊ8-5=3���ʱ�ΪFԪ�أ���ΪAl��
A����ΪNԪ�أ���Ԫ�ص��������5�����ӣ����⻯�ﺬ��N-H���Լ�����A��ȷ��
B������Ԫ���б���F���ķǽ�������ǿ������Ԫ��û����ۺ����ᣬ��B����
C����Ԫ�ص��������Ӧ��ˮ����Ϊ������������Ԫ������������Ӧˮ����Ϊ���ᣬ����ǡ����ȫ��Ӧ��������������Һ��������ˮ�⣬��Һ�����ԣ���C��ȷ��
D���ҡ�����Ԫ���γɵļ��⻯��ֱ�ΪNH3��HF�����ڷ�Ԫ�طǽ����Խ�ǿ����HF���ȶ��ԱȰ���ǿ����D��ȷ��
��ѡB��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ؼ����жϸ�Ԫ���������ڡ���Ԫ���������壬�Դ˽����ƶϣ��Ѷ��еȣ�


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����仯�����ڹ��õķ�չ��������Ҫ���ã�
�����仯�����ڹ��õķ�չ��������Ҫ���ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��Q������������Ӧ��ˮ�������Ա�W��ǿ | |
| B�� | ������W2Q2�У���ԭ����������8���ӽṹ | |
| C�� | ��ҵ��ͨ�����Z��Q�γɵĻ������Ʊ�Z���� | |
| D�� | Y������X����̬�⻯��ɷ����û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼúΪȼ�������Լ��ٶ���������к�������ŷţ����������������Ĵ�ʩ֮һ | |
| B�� | ʯӢ��̹�����������Ũ�����ǿ��ʴ�� | |
| C�� | ��ֽ�ˮ��������ֲ��ո����������������Ҵ��漰���������ܵ����� | |
| D�� | Ӳ����̼�ظֶ��ǺϽ���ϣ��ϳ���ά�����ά�����л��߷��ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���н�����һ����Ӧ | |
| B�� | Fe3+�ܴ�H2O2�ķֽ� | |
| C�� | ��Ӧ��������ҺpH���ϼ�С | |
| D�� | FeSO4������ʵ�����H2O2ǡ�÷�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mo1 Na2O2������������ | |
| B�� | 1 L0.1 mol•L-1��ˮ�е�NH${\;}_{4}^{+}$ | |
| C�� | 12.5mL 16 mo1•L-1��Ũ�������ܽ��Cu | |
| D�� | 4.6g N02���������ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
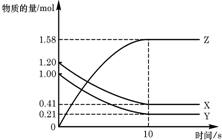 һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ����ش��������⣺
һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com