
【题目】Ⅰ、 下列各组物质:①O2和O3 ②H2、D2、T2 ③12 C和14 C ④CH3CH2CH2CH3和(CH3)2CHCH3 ⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 (在横线上填相应的序号)
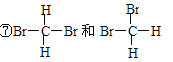
A、互为同位素的是_________ ;B、互为同分异构体的是________;
C、互为同素异形体的是________;D、同一种物质的是_________。
Ⅱ.写出下列反应的化学方程式,并注明反应类型
①乙烯通入到溴的四氯化碳溶液中:_____________________,反应类型___________。
②苯与浓硝酸、浓硫酸混合后加热至50℃~60℃发生反应:__________________,反应类型 ___________________。
【答案】 ③ ④⑥ ① ②⑦ CH2=CH2+Br2→CH2BrCH2Br 加成反应 ![]()
![]() 取代反应
取代反应
【解析】试题分析:Ⅰ、质子数相同、中子数不同的原子互为同位素; 分子式相同,结构不同的有机物互为同分异构体;同种元素组成的性质不同的单质互为同素异形体; D、分子式、结构都相同的物质是同一种物质。Ⅱ.①乙烯与溴的四氯化碳溶液发生加成反应,生成1,2-二溴乙烷。②苯与浓硝酸、浓硫酸混合后加热至50℃~60℃发生取代反应,生成溴苯。
解析:根据以上分析:Ⅰ、A、③12 C和14 C互为同位素; B、④CH3CH2CH2CH3和(CH3)2CHCH3 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5互为同分异构体;
C、①O2和O3互为同素异形体; D ②H2、D2、T2、 是同一种物质。Ⅱ.①乙烯与溴的四氯化碳溶液发反应,生成1,2-二溴乙烷,方程式为CH2=CH2+Br2→CH2BrCH2Br,属于加成反应。②苯与浓硝酸、浓硫酸混合后加热至50℃~60℃发生反应,生成溴苯,方程式为
是同一种物质。Ⅱ.①乙烯与溴的四氯化碳溶液发反应,生成1,2-二溴乙烷,方程式为CH2=CH2+Br2→CH2BrCH2Br,属于加成反应。②苯与浓硝酸、浓硫酸混合后加热至50℃~60℃发生反应,生成溴苯,方程式为![]()
![]() ,属于取代反应。
,属于取代反应。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其工作原理如图所示。下列说法中不正确的是

A. 电池放电时Na+从a极区移向b极区
B. 燃料电池是一类能量转化效率高、环境友好的发电装置
C. 该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O
D. 在电池反应中,每消耗3molH2O2,转移电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应CO+H2O(g)CO2+H2在1000K达到平衡时,分别改变下列条件,K值发生变化的是( )
A.将压强减小至原来的一半
B.添加催化剂
C.将反应温度升高至1200 K
D.增大水蒸气的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,图甲是镁-次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是

A. 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
B. 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合,转化成Cr(OH)3除去
C. 图乙电解池中,若有0.84 g阳极材料参与反应,则阴极会有168 mL(标准状况)的气体产生
D. 若图甲燃料电池消耗0.36 g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2O2(1)=2H2O(1)+O2(g)反应过程中的能量变化曲线如图所示,下列说法不正确的是

A. 该反应的△H<0,△S>0
B. 途径Ⅱ与途径I相比,可能是加了催化剂
C. 其他条件相同时,产生相同体积的氧气时放出的热量:途径I >途径Ⅱ
D. 其他条件相同时,产生相同体积的氧气所需的时间:途径I>途径Ⅱ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物对人类的生产和生活有着重要的作用。
(1)重晶石(BaSO4)高温煅烧可发生一系列反应,其中部分反应如下:
BaSO4(s)+4C(s)=BaS(s)+4CO(g) ΔH=+571.2kJ·mol-1
BaS(s)=Ba(s)+S(s) ΔH=+460kJ·mol-1
已知:O2(g)+2C(s)=2CO(g) ΔH=-221kJ·mol-1,
写出O2氧化Ba(s)和S(s)至BaSO4的热化学方程式___________________。
(2)一定条件下,通过下列反应可实现燃煤烟气中硫的回收:2CO(g)+SO2(g)![]() 2CO2(g)+S(l) △H<0。若向2L恒容密闭容器中通入2molCO和1molSO2,反应在不同条件下进行上述反应,反应体系总压强随时间的变化如图所示
2CO2(g)+S(l) △H<0。若向2L恒容密闭容器中通入2molCO和1molSO2,反应在不同条件下进行上述反应,反应体系总压强随时间的变化如图所示
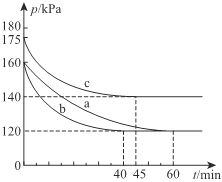
①与实验a相比,c组改变的实验条件可能是______________,判断的依据是______________________。
②用P0表示开始时总压强,P表示平衡时总压强,用α表示SO2的平衡转化率,则α的表达式为______________________。
(3)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)![]() SO3(g)+NO(g) ΔH=-42kJ·mol-1。
SO3(g)+NO(g) ΔH=-42kJ·mol-1。
在1 L 恒容密闭容器中充入SO2(g) 和NO2 (g),所得实验数据如下:
实验 编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(SO2) | n(NO2) | n(NO) | ||
甲 | T1 | 0.80 | 0.20 | 0.18 |
乙 | T2 | 0.20 | 0.80 | 0.16 |
丙 | T2 | 0.20 | 0.30 | a |
①实验甲中,若2 min 时测得放出的热量是4.2 kJ,则0~2 min时间内,用SO2 (g)表示的平均反应速率υ(SO2)=__________,该温度下的平衡常数为______________。
②实验丙中,达到平衡时,NO2的转化率为_______________。
③由表中数据可推知,T1_____T2(填“>”“<”或“=”),判断的理由是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中处处有化学,下列有关说法正确的是( )
A.淀粉和纤维素均为天然高分子化合物
B.饮用矿泉水瓶的主要成分是聚氯乙烯
C.凡含有食品添加剂的食物均不可食用
D.大米煮成粥后,淀粉就变成了葡萄糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com