
【题目】用0.1500mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示,
实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
1 | 25.00 | 24.41 |
2 | 25.00 | 24.39 |
3 | 25.00 | 25.60 |
回答下列问题:
(1)实验中,需要润洗的仪器是:________________________(填写仪器名称)。
(2)取待测液NaOH溶液25.00ml 于锥形瓶中,使用酚酞做指示剂。滴定终点的判断依据是______________
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则消耗盐酸溶液的体积为________mL。

(4)下列操作中会使所测结果偏高的是_________________、偏低的是_________________
①酸式滴定管漏液;②滴定前酸式滴定管尖嘴部分有气泡,滴定过程中气泡变小;③滴定过程中,振荡锥形瓶时,不小心将溶液溅出;④滴定过程中,锥形瓶内加少量蒸馏水; ⑤用甲基橙作指示剂进行滴定时,溶液由橙色变红色时停止滴定;⑥用甲基橙作指示剂,溶液由黄色变橙色,5 s后又变为黄色。⑦读酸式滴定管读数时,滴定前仰视读数
(5)未知浓度的NaOH溶液的物质的量浓度为_____________mol/L。
【答案】酸式滴定管、碱式滴定管 滴入最后一滴标准液,溶液由红色变为无色,且半分钟内不恢复红色 26.10 mL ①②⑤ ③⑥⑦ 0.1464mol/L
【解析】
(1)根据滴定管不用待盛装的溶液润洗,相当于给溶液稀释;盛装待测液的锥形瓶不能使用待测液润洗,否则待测液的物质的量偏大;
(2)用酚酞作指示剂时,滴定前,酚酞遇碱变红,到达滴定终点时观察到溶液颜色由红变为无色;
(3)根据滴定管的构造进行读数,注意平视;
(4)根据c(待测)=![]() 进行判断;
进行判断;
(5)根据c(待测)=![]() 计算未知浓度的NaOH溶液的物质的量浓度c(待测)。
计算未知浓度的NaOH溶液的物质的量浓度c(待测)。
(1)实验中,酸式滴定管、碱式滴定管需要用待盛装的溶液润洗,否则会被水稀释,锥形瓶不能使用待测液润洗,否则待测液的物质的量偏大;故需要润洗的仪器是:酸式滴定管、碱式滴定管;
(2)碱溶液中滴加无色酚酞,碱能使酚酞变红,故利用酚酞作指示剂,滴定达到终点的现象是酚酞的红色褪去且半分钟不再出现红色,则滴定终点的判断依据是滴入最后一滴标准液,溶液由红色变为无色,且半分钟内不恢复红色;
(3)起始读数为0.00mL,终点读数为26.10mL,盐酸溶液的体积为26.10mL;
(4)①酸式滴定管漏液,造成V(标准)偏大,根据c(待测)=![]() ,可知c(标准)偏高;
,可知c(标准)偏高;
②滴定前酸式滴定管尖嘴部分有气泡,滴定过程中气泡变小,造成V(标准)偏大,根据c(待测)=![]() ,可知c(标准)偏高;
,可知c(标准)偏高;
③滴定过程中,振荡锥形瓶时,不小心将溶液溅出,造成待测液损失,根据c(待测)=![]() ,可知c(标准)偏低;
,可知c(标准)偏低;
④滴定过程中,锥形瓶内加少量蒸馏水,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=![]() ,可知c(标准)不变;
,可知c(标准)不变;
⑤用甲基橙作指示剂进行滴定时,溶液由橙色变红色时停止滴定,造成V(标准)偏大,根据c(待测)=![]() ,可知c(标准)偏高;
,可知c(标准)偏高;
⑥用甲基橙作指示剂,溶液由黄色变橙色,5 s后又变为黄色,造成V(标准)偏小,根据c(待测)=![]() ,可知c(标准)偏低;
,可知c(标准)偏低;
⑦读酸式滴定管读数时,滴定前仰视读数,造成V(标准)偏小,根据c(待测)=![]() ,可知c(标准)偏低;
,可知c(标准)偏低;
综上,操作中会使所测结果偏高的是①②⑤、偏低的是③⑥⑦;
(5)根据数据的有效性,舍去第3组数据,然后求出1、2组平均消耗V(盐酸)=24.40mL,
HCl+NaOH=NaCl+H2O
0.02440L×0.1000mol/L 0.025L×c(NaOH)
则c(NaOH)=![]() =0.1464mol/L。
=0.1464mol/L。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A.0.1mol·L-1KI溶液:Na+、K+、ClO-、OH-
B.0.1mol·L-1Fe2(SO4)3溶液:Cu2+、![]() 、
、![]() 、
、![]()
C.0.1mol·L-1HCl溶液:Ba2+、K+、CH3COO-、![]()
D.0.1mol·L-1NaOH溶液:Mg2+、Na+、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应aA(g)+bB(g)![]() cC(g) H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:
cC(g) H<0,在体积为2L的密闭容器中反应:在I、II、III不同阶段体系中改变某一条件,体系中各物质的量(mol)随时间变化的曲线如图所示。下列说法不正确的是:
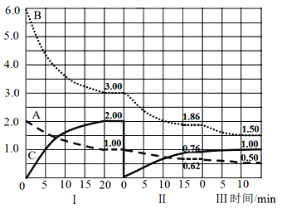
A.该反应的化学反应方程式为:A+3B![]() 2C
2C
B.用物质A表示第I阶段20分钟内平均反应速率为:v(A)=0.025mol·L-1·min-1
C.三个阶段反应的平衡常数关系为:KI<KII<KIII
D.三个阶段反应的速率为:v(B)I>v(B)II>v(B)III,各段内转化率AI%>AII%>AIII%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种常用香料的主要成分之一,其合成路线如下。
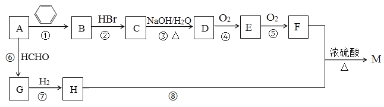
已知:
①相同条件下1体积烃A完全燃烧消耗4体积氧气;
②RC≡CH+HCHO![]() RC≡CCH2OH;
RC≡CCH2OH;
③反应①的原子利用率为100%,反应类型属于加成反应;
④M的分子式为C13H18O2。
回答下列问题:
(1)A的名称为___________;G分子中有___ _个碳原子在同一条直线上。
(2)反应②~⑧中属于加成反应的是______;H中官能团的名称为___________。
(3)物质M的结构简式为____________。B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为_____________。
(4)反应③的化学反应方程式为_______________。
(5)符合下列条件的F的同分异构体共有_____种。
①能发生银镜反应;②能发生水解反应;③属于芳香族化合物。
其中核磁共振氢谱为4组峰,且峰面积之比为6∶2∶1∶1的为 (任写一种物质的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某溶液中由水电离产生的c(H+)和c(OH-)的乘积为1×10-20,下列说法正确的是
A.该溶液的pH一定是10B.该溶液不可能pH=4
C.该溶液的pH不可能是7D.不会有这样的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于难溶电解质溶解平衡的说法正确的是
A. 可直接根据 Ksp 的数值大小比较难溶电解质在水中的溶解度大小
B. 在 AgCl 的饱和溶液中,加入蒸馏水, Ksp(AgCl)不变
C. 难溶电解质的溶解平衡过程是可逆的,且在平衡状态时 v溶解=v沉淀=0
D. 25℃时, Ksp(AgCl)>Ksp(AgI),向 AgCl 的饱和溶液中加入少量 KI 固体,一定有黄色沉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X是一种医药中间体,其结构简式如图所示。下列有关该有机物的叙述正确的是![]()
![]()

A.有机物X的分子式为![]()
B.该有机物能够发生酯化反应、水解反应和消去反应
C.分子内所有碳原子可能处于同一平面
D.该有机物与NaOH反应,最多消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①2C(s)+O2(g)=2CO(g) ΔH=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol
下列结论正确的是( )
A.碳的燃烧热为ΔH=-221kJ/mol
B.1molC(s)和0.5molO2(g)所具有的能量高于1molCO(g)所具有的能量
C.稀硫酸与稀NaOH溶液反应放出的热量为57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量大于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组拟以对苯二酚为原料合成染料G。合成路线如下:
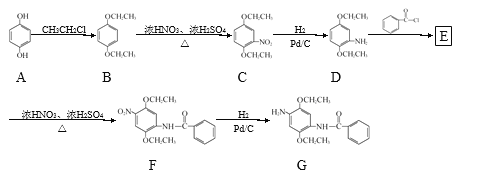
![]()
![]() 中的含氧官能团名称为________、________。
中的含氧官能团名称为________、________。
![]() 的反应类型为________。
的反应类型为________。
![]() 的分子式为
的分子式为![]() ,写出E的结构简式:________。
,写出E的结构简式:________。
![]() 的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
![]() 含有苯环,且分子中有一个手性碳原子,能与
含有苯环,且分子中有一个手性碳原子,能与![]() 溶液发生显色反应;
溶液发生显色反应;![]() 能发生水解反应,水解产物均有4种不同环境的氢且水解产物之一是
能发生水解反应,水解产物均有4种不同环境的氢且水解产物之一是![]() 氨基酸。
氨基酸。
![]() 已知:
已知:![]() 苯胺
苯胺![]()
![]()
![]() 易被氧化;
易被氧化;![]()
![]()
![]()
![]()
![]() ,写出以
,写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图________(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图________(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com