
| A.重油的裂化 | B.硝酸使蛋白质变性 |
| C.煤的干馏 | D.石油的分馏 |
科目:高中化学 来源:不详 题型:单选题
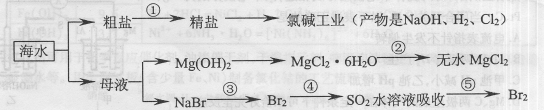
| A.在工段③和⑤中需要用到氯碱工业的产物 |
| B.工段②中的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| C.大量的含Fe3+废水排人海洋,易引发赤潮 |
| D.工段①中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液一过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在电解铝工业中添加冰晶石 |
| B.研制出性能优良的催化剂,降低反应所需温度 |
| C.开发太阳能、风能、氢能等清洁能源 |
| D.大力发展火电,缓解用电紧张 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
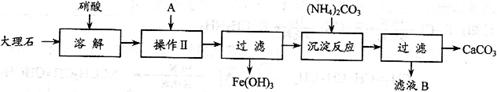
 , 若A为溶液,则A可以是 。
, 若A为溶液,则A可以是 。 。
。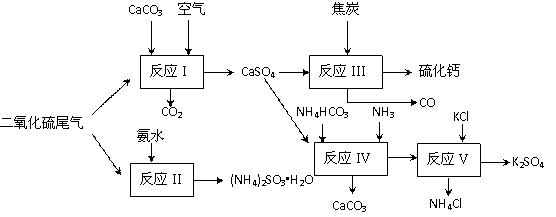
| A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙 |
B.反应Ⅲ中发生反应的化学方程式为:CaSO4+4C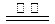 CaS +4CO↑ CaS +4CO↑ |
| C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解 |
| D.反应Ⅴ中的副产物氯化铵可用作氮肥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.光导纤维是以二氧化硅为主要原料制成的 |
| B.大气中二氧化碳的含量增加是酸雨的形成主要原因 |
| C.在西部和沿海地区兴建风力发电站,解决能源短缺问题 |
D.推广利用微生物发酵技术, 将植物桔杆、动物粪便等制成沼气以替代液化石油气符合“低碳经济” 将植物桔杆、动物粪便等制成沼气以替代液化石油气符合“低碳经济” |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
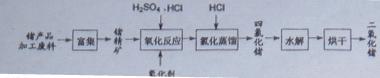
 2O2反应生成Ge4+,写出该反应的离子方程式 。
2O2反应生成Ge4+,写出该反应的离子方程式 。 (2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是 。实验室蒸馏操作时常用的玻璃仪器有:酒精灯、蒸馏烧瓶、 、 、接收管、锥形瓶等。
(2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是 。实验室蒸馏操作时常用的玻璃仪器有:酒精灯、蒸馏烧瓶、 、 、接收管、锥形瓶等。 。
。

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
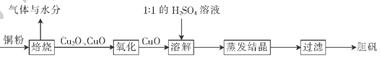
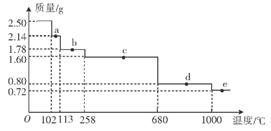
| A.加人稀H2SO4,若溶液呈蓝色,说明固体中一定有CuO |
| B.加人稀H2SO4,若有红色沉淀物生成,说明固体中一定有Cu2O |
| C.加人稀HNO3,若有无色气体(随即变成红棕色:)产生,说明固体中有Cu2O |
| D.加人稀HNO3,若固体全部溶解,说明固体中没有Cu2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开发核能、太阳能、氢能等新能源,使用无磷洗涤剂都可直接降低碳排放 |
| B.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 |
| C.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能 |
| D.针对节能减排需要大力建设火电厂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.能全部透过半透膜 | B.有丁达尔效应 |
| C.不能透过滤纸 | D.所得分散系一定是浊液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com