
 ;
; +2C2H5OH$?_{△}^{浓硫酸}$
+2C2H5OH$?_{△}^{浓硫酸}$ +2H2O.
+2H2O. 、
、 .
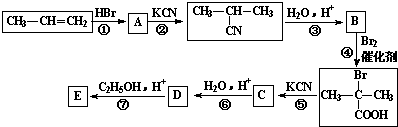
. 分析 丙烯与HBr发生加成反应生成A,A为溴代烷,A与KCN发生取代反应,生成 ,故A为
,故A为 ,由信息②,可知B为
,由信息②,可知B为 ,
,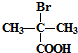 与KCN发生取代反应生成C,C为
与KCN发生取代反应生成C,C为 ,C$\stackrel{H_{2}O/H+}{→}$D,由信息RCN$\stackrel{H_{2}O/H+}{→}$RCOOH可知D为
,C$\stackrel{H_{2}O/H+}{→}$D,由信息RCN$\stackrel{H_{2}O/H+}{→}$RCOOH可知D为 ,
, 与足量的乙醇发生酯化反应生成E,E为
与足量的乙醇发生酯化反应生成E,E为 ,据此分析解答.
,据此分析解答.
解答 解:丙烯与HBr发生加成反应生成A,A为溴代烷,A与KCN发生取代反应,生成 ,故A为
,故A为 ,由信息②,可知B为
,由信息②,可知B为 ,
,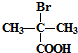 与KCN发生取代反应生成C,C为
与KCN发生取代反应生成C,C为 ,C$\stackrel{H_{2}O/H+}{→}$D,由信息RCN$\stackrel{H_{2}O/H+}{→}$RCOOH可知D为
,C$\stackrel{H_{2}O/H+}{→}$D,由信息RCN$\stackrel{H_{2}O/H+}{→}$RCOOH可知D为 ,
, 与足量的乙醇发生酯化反应生成E,E为
与足量的乙醇发生酯化反应生成E,E为 ,
,
(1)由上述分析可知,A的结构简式为  ,故答案为:
,故答案为: ;
;
(2)反应④是取代反应,
故答案为:取代反应;
(3)反应④的方程式为CH3CH(CH3)COOH+Br2$\stackrel{催化剂}{→}$CH3CBr(CH3)COOH+HBr,
故答案为:CH3CH(CH3)COOH+Br2$\stackrel{催化剂}{→}$CH3CBr(CH3)COOH+HBr;
(4) 与足量的乙醇发生酯化反应生成
与足量的乙醇发生酯化反应生成 ,反应化学方程式为:
,反应化学方程式为: +2C2H5OH$?_{△}^{浓硫酸}$
+2C2H5OH$?_{△}^{浓硫酸}$ +2H2O,
+2H2O,
故答案为: +2C2H5OH$?_{△}^{浓硫酸}$
+2C2H5OH$?_{△}^{浓硫酸}$ +2H2O;
+2H2O;
(5) 的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为:
的同分异构体有多种,其中既能发生银镜反应,又能发生酯化反应,说明分子中含有醛基-CHO与羟基-OH,符合结构的有机物为: 、
、 等
等
故答案为: ;
; .
.
点评 本题考查有机推断与合成,侧重考查学生分析推断及知识综合应用能力,涉及烯烃、卤代烃、醇、羧酸的性质以及根据信息进行的反应等,是对有机化合物知识的综合考查,利用给出的反应信息推断A的结构是解题的关键,然后利用顺推法推断其它物质,题目难度中等.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | 漂白粉、氯化钾、硫酸钡 | B. | 氯水、次氯酸钠、乙醇 | ||
| C. | 液氯、胆矾、干冰 | D. | 重水、烧碱、水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
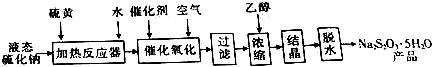
| 溶液温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 氧化完全所需时间/h | 6 | 5.5 | 5.5 | 6 | 20 | 16 | 11 | 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 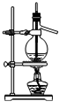 石油的分馏 | B. | 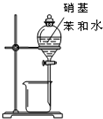 分离硝基苯和水 | ||
| C. | 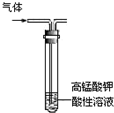 除去甲烷中的乙烯 | D. | 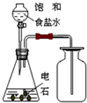 制取并收集乙炔气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,KW增大,pH不变 | |
| B. | 向水中加入氨水,平衡向逆反应方向移动,c(OH-)降低 | |
| C. | 向水中加入少量氯化铵,c(H+)增大 | |
| D. | 向水中加入少量固体CH3COONa,平衡向逆反应方向移动,c(H+)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸与氢氧化钡在溶液中反应Ba2++SO42-═BaSO4↓ | |
| B. | 氢氧化镁溶于稀硫酸:2H++Mg(OH)2═Mg2++2H2O | |
| C. | 大理石与盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| D. | 少量金属钠投入到CuSO4溶液中 2Na+Cu2+═2Na++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{2}^{3}$He原子核内有2个中子 | |
| B. | ${\;}_{2}^{3}$He原子核外有3个电子 | |
| C. | ${\;}_{2}^{3}$He原子核内有3个质子 | |
| D. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He是两种不同的核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
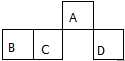 短周期元素A、B、C、D在元素周期表中的相对位置如图.其中A原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
短周期元素A、B、C、D在元素周期表中的相对位置如图.其中A原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 原子半径:rD>rC>rB>rA | |
| B. | 含D元素的盐溶液一定显中性 | |
| C. | 氢化物的热稳定性:C>D | |
| D. | D的单质能与A形成的氢化物反应生成具有漂白性的物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com