

分析 Ⅰ.(1)在加热条件下,用液态肼(N2H4)还原新制的Cu(OH)2制备Cu20,同时放出N2,结合质量守恒定律和氧化还原反应可写出此反应的化学方程式;
(2)根据“Cu+易在酸性条件下发生反应:2Cu+=Cu2++Cu”写出反应的离子方程式;
Ⅱ.工业废渣(主要成分为硅,铜,碳等)焙烧后得固体为硅和铜的氧化物,用盐酸浸取后得氯化铜溶液和二氧化硅固体,过滤得滤渣为SiO2,滤液为氯化铜溶液,滤液中加氢氧化钠调节PH值为3.5,再加亚硫酸钠还原得氯化亚铜沉淀,过滤后得滤饼,对滤饼的醇洗,干燥,得氯化亚铜晶体,据此答题.
解答 解:Ⅰ.(1)根据反应物N2H4和Cu(OH)2,生成物是Cu20、H2O和N2,可得化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;加热\;}}{\;}$N2↑+2Cu2O+6H2O,故答案为:4Cu(OH)2+N2H4$\frac{\underline{\;加热\;}}{\;}$N2↑+2Cu2O+6H2O;
(2)氧化亚铜(Cu2O)在酸性条件下不稳定,生成Cu和Cu2+,反应的离子方程式为:Cu2O+2H+═Cu+Cu2++H2O,
故答案为:Cu2O+2H+═Cu+Cu2++H2O;
Ⅱ.工业废渣(主要成分为硅,铜,碳等)焙烧后得固体为硅和铜的氧化物,用盐酸浸取后得氯化铜溶液和二氧化硅固体,过滤得滤渣为SiO2,滤液为氯化铜溶液,滤液中加氢氧化钠调节PH值为3.5,再加亚硫酸钠还原得氯化亚铜沉淀,过滤后得滤饼,对滤饼的醇洗,干燥,得氯化亚铜晶体,
(1)根据上面的分析可知,“滤渣”的主要成分为SiO2,
故答案为:SiO2;
(2)“还原”过程中SO32-将Cu2+还原为CuCl,反应的离子方程式为:2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H﹢,亚硫酸钠需适当过量,防止生成的CuCl被氧化,
故答案为:2Cu2++SO32-+2Cl-+H2O=2CuCl↓+SO42-+2H﹢;防止生成的CuCl被氧化;
(3)操作Ⅰ和操作Ⅱ均为过滤,所用的玻璃仪器为漏斗、烧杯、玻璃棒,使用无水乙醇代替水进行洗涤的优点是 减小洗涤CuCl时的溶解损失并防止其水解氧化,
故答案为:漏斗、烧杯、玻璃棒; 减小洗涤CuCl时的溶解损失并防止其水解氧化;
(4)CuCl是共价化合物,经测定其蒸气对H2的相对密度为99.5,则其相对分子质量为199,结合实验室为CuCl计算(CuCl)n=199,n=2得到化学式Cu2Cl2,
故答案为:Cu2Cl2.
点评 本题考查了物质的分离提纯实验过程分析判断、题干信息的应用、氧化还原反应产物的分析及其离子和化合物性质的理解应用等知识点,注意知识的迁移和应用是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、OH-、C1- | B. | Ba2+、K+、CO32-、NO3- | ||
| C. | Na+、K+、C1-、HCO3- | D. | H+、Na+、C1-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的体积之比为1:1 | B. | 它们所含氧原子数目之比为2:3 | ||
| C. | 它们的分子数目之比为1:1 | D. | 它们所含原子数目之比为3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验后剩余的钠粒,需要放回原试剂瓶中 | |
| B. | 自然界中钠只能以化合物的形式存在 | |
| C. | 钠的化学性质比较活泼,少量的钠可以保存在与钠不反应的煤油中 | |
| D. | 当钠与硫酸铜溶液反应时,有大量红色固体铜出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用食品添加剂与提倡绿色食品相违背 | |
| B. | 含有食品添加剂的食品应该少食,以防中毒 | |
| C. | 没有加任何添加剂的天然食品是最安全的 | |
| D. | 食品添加剂在合理限量范围内不影响人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
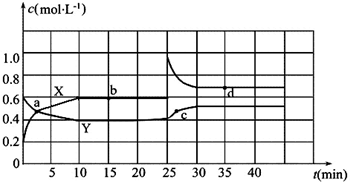
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
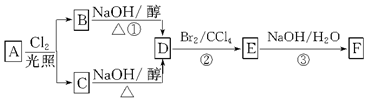
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com