
| A. | 二氧化碳分子的电子式: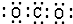 | B. | HClO的结构式为 H-Cl-O | ||
| C. | 硅的原子结构示意图: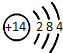 | D. | 甲烷分子的比例模型: |
分析 A、二氧化碳分子中碳原子与氧原子之间形成2对共用电子对;
B、HClO分子中O形成2对共用电子对;
C、硅原子的核内有14个质子,核外有14个电子;
D、 为甲烷的球棍模型.
为甲烷的球棍模型.
解答 解:A、二氧化碳分子中碳原子与氧原子之间形成2对共用电子对,电子式为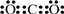 ,故A错误;
,故A错误;
B、HClO分子中O形成2对共用电子对,则HClO分子的结构式为H-O-Cl,故B错误;
C、硅原子的核内有14个质子,核外有14个电子,故硅的原子的结构示意图为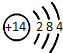 ,故C正确;
,故C正确;
D、甲烷分子的比例模型应该体现出甲烷分子中各原子的相对体积大小, 为甲烷的球棍模型,甲烷的比例模型为:
为甲烷的球棍模型,甲烷的比例模型为: ,故D错误.
,故D错误.
故选C.
点评 本题考查了化学基本概念的理解和应用,熟悉电子式、比例模型和球棍模型的区别、结构示意图等即可判断,掌握物质的组成和结构是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:HX>H2Y>ZH3 | |
| B. | 非金属活泼性:Z<Y<X | |
| C. | 单质的氧化性:X2>Y>Z | |
| D. | X与Z形成的化合物均能达8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做银镜反应后的试管用氨水洗涤 | |
| B. | 苯酚如不慎沾到皮肤上,应立即用酒精洗涤 | |
| C. | 乙酸乙酯与稀硫酸混合水浴加热,酯层完全消失 | |
| D. | 向2mL10%硫酸铜溶液滴加4~6滴2%氢氧化钠溶液中,再加入0.5mL乙醛溶液加热,有红色沉淀出现 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 | |
| B. | 某元素一种同位素原子的质子数为m,中子数为n.则这种元素的相对原子质量为m+n | |
| C. | 同种元素的原子均有相同的质子数和中子数 | |
| D. | 仅由两种元素形成的共价化合物中可以同时含有极性共价键和非极性共价键强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能发生氧化反应 | |
| B. | 至少有三种同分异构体可以水解得到甲酸或甲醇 | |
| C. | 至少有三种同分异构体能与NaOH溶液反应 | |
| D. | 分子中含有碳碳双键或碳氧双键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com