
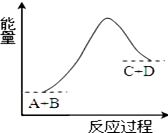
| A. | 该反应只有在加热条件下才能进行 | |
| B. | 该反应中D的能量可能大于反应物A和B的能量之和 | |
| C. | 该反应为放热反应 | |
| D. | 反应物的总能量高于生成物的总能量 |
分析 A.某些吸热反应不需要加热也可以发生;
B.图象分析可知反应过程中反应物能量低于生成物;
C.依据图象分析反应物能量低于生成物,结合能量守恒分析判断反应能量变化;
D.由图可知,此反应物的总能量低于生成物的总能量.
解答 解:A.某些吸热反应不需要加热也可以发生,如氢氧化钡晶体和铵盐发生的吸热反应,故A错误;
B.图象分析可知反应过程中反应物能量一定生成物能量(C和D的总能量),D的总能量可能高于A和B的总能量之和,故B正确;
C.图象分析反应物能量低于生成物,结合能量守恒分析反应是吸热反应,故C错误;
D.反应物的总能量低于生成物的总能量,故D错误,故选B.
点评 本题考查了化学反应能量变化分析,图象分析方法和应用,注意反应吸热放热和反应条件关系的判断应用,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入盐酸,产生的气体能使石灰水变浑浊,该溶液中一定含有CO32- | |
| B. | 某溶液中加入硝酸酸化的BaCl2,产生白色沉淀,该溶液中一定含有SO42- | |
| C. | 用洁净的铂丝蘸取某溶液在酒精灯上灼烧,产生黄色火焰,溶液中一定含Na+,一定不含K+ | |
| D. | 某溶液中加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,该溶液中一定含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
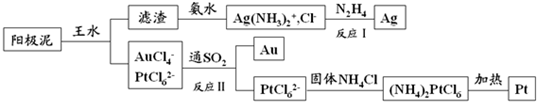
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
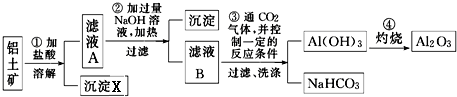
 .
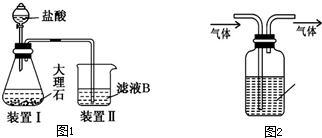
.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将a molL-1 HCN溶液与a molL-1 NaOH溶液等体积混合,混合液中:c(OH-)>c(H+),c(Na+)>c(CN-) | |
| B. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| C. | 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| D. | NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L的苯所含的分子个数为0.5NA | |
| B. | 28 g乙烯所含共用电子对数目为4NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含原子个数为2.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子个数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com