
【题目】等质量两份铝,分别放入足量盐酸和NaOH 中,生成氢气在同温同压下体积比为( )
A.2:3
B.3:2
C.1:1
D.1:6
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】(Ⅰ)有以下10种物质:①液态氯化氢、②CCl4、③液氯、④硫酸铵晶体、⑤铁、⑥稀硫酸、⑦澄清石灰水、⑧二氧化硫,⑨熔融的硫酸钠、⑩Na2O固体。其中属于电解质的是_______(填序号,下同),属于非电解质的是_________,在现状态下能导电的是__________,写出④在水溶液中电离的方程式__________。
(Ⅱ)A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)C的离子结构示意图为_________;
(2)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铬与铁具有相似的化学性质。醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O(摩尔质量376g/mol)是一种氧气吸收剂,红棕色晶体,易被氧化;易溶于盐酸,微溶于乙醇,难溶于水和乙醚。其制备装置(已省略加热及支持装置)和步骤如下:
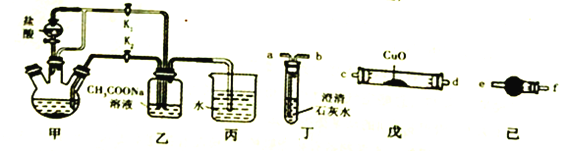
I.组装实验仪器后,首先进行必要的操作A。
II.往三颈烧瓶中依次加入过量锌粒、适量CrCl3溶液,再往其它仪器中加入相应的药品。
III.关闭K2,打开K1,旋开分液漏斗的旋塞并控制好滴速。
IV.待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,把溶液自动转移到装置乙中,当出现大量红棕色晶体时,关闭分液漏斗旋塞。
V.将装置乙中混合物快速过滤、洗涤和干燥,称量。
回答下列问题:
(1)步骤I中“操作A”为_____________;装置丙中导管口水封的目的主要是_________________________________。
(2)三颈烧瓶中的锌除与盐酸反应外,另发生的一个反应的化学方程式为_______________。
(3)步骤IV中溶液自动转移至装置乙中的实验操作为_______________;生成红棕色晶体的离子反应方程式____________________________。
(4)为得到纯净干燥的产品,洗涤时按使用的先后顺序选用下列洗涤剂__________(填序号)。
①乙醚②蒸馏水(煮沸冷却) ③无水乙醇 ④盐酸
(5)一定条件下[Cr(CH3COO)2]2·2H2O受热反应得到的气态产物含CO、CO2。请从丁、戊、己装置中选取必要装置检验这两种气体(不考虑尾气处理):
气态产物→_______________________→a(填接口字母序号)。
(6已知实验所用到的试剂中,CrCl3溶液中含溶质19.02g,0.1mol/L醋酸钠溶液为1.6L,其它反应物足量。实验后得到纯净干燥的[Cr(CH3COO)2]2·2H2O晶体11.28g,则该实验所得产品的产率为________(结果保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年采用中国自主知识产权的全球首套煤基乙醇工业化项目投产成功。某地用煤制乙醇的过程表示如下。

(1)Cu(NO3)2是制备“催化剂X”的重要试剂。

①气体A是_________。
②实验室中用Cu(NO3)2固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3的作用: ________。
③NaClO溶液吸收气体A的离子方程式是_________。
(2)过程a包括以下3个主要反应:
I.CH3COOCH3(g)+2H2(g)![]() C2H5OH(g)+CH3OH(g) △H1
C2H5OH(g)+CH3OH(g) △H1
II.CH3COOCH3(g)+C2H5OH(g)![]() CH3COOC2H5(g)+CH3OH(g) △H2
CH3COOC2H5(g)+CH3OH(g) △H2
III.CH3COOCH3(g)+H2(g)![]() CH3CHO(g)+CH3OH(g) △H3
CH3CHO(g)+CH3OH(g) △H3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性(如乙醇的选择性= ![]() )如下图所示。
)如下图所示。

①已知:△H1<0。随温度降低,反应I化学平衡常数的变化趋势是________。
②下列说法不合理的是_______。
A.温度可影响反应的选择性
B.225℃~235℃,反应I处于平衡状态
C.增大H2的浓度,可以提高CH3COOCH3的转化率
③为防止“反应III”发生,反应温度应控制的范围是____________。
④在185℃,上述反应中CH3COOCH3起始物质的量为5mol,生成乙醇的物质的量是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液:
(1)求所得盐酸的物质的量浓度_____
(2)若将此溶液再稀释成1L溶液,求稀释后盐酸的物质的量浓度_____
(3)将(2)的溶液取出500mL与足量的Zn反应可以产生多少体积的H2(在标准状况下)_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是主要大气污染物之一,工业上可用如图装置吸收转化SO2(A、B 为惰性电极)。下列说法错误的是( )

A. a为电源的正极
B. B 极上发生氧化反应
C. 离子交换膜为阳离子交换膜
D. A极区溶液的pH逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型中温全瓷铁一空气二次电池,其结构如图所示。下列有关该电池的说法正确的是

A. 放电时O2-从a移向b B. 放电时负极的电极反应为O2+4e-=2O2-
C. 充电时1molFe 氧化为FeOx,转移2xmole- D. 充电时a 与电源的负极相连。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸乙酯具有抗炎作用且有治疗自身免疫性疾病的潜力,其合成路线如图所示:
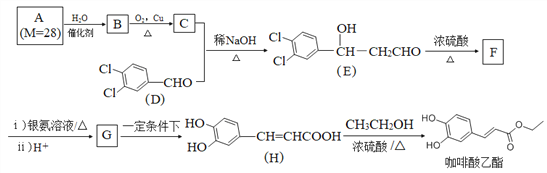
回答下列问题:
(1)C+D→E反应类型为______。F中含氧官能团的名称是______。
(2)D分子中位于同一平面上的原子最多有______个。G的结构简式为______。
(3)H→咖啡酸乙酯的化学方程式为______。
(4)芳香族化合物M是H的同分异构体,1 molM与足量碳酸氢钠溶液反应生成2 molCO2,M的结构有______种;其中核磁共振氢谱为5组峰,峰面积比为1∶2∶2∶2∶1的结构简式为______。
(5)以上图中的C和甲醛为原料,设计合成C5H12O4(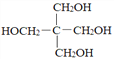 )的路线(无机试剂任任选)。________________________
)的路线(无机试剂任任选)。________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com