
 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
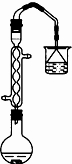
)为原料制备2-氯丁烷 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
分析 步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L-1浓盐酸,充分溶解、冷却,再加入2一丁醇,加热一段时间反应生成2-氯丁烷,氯化锌是催化剂;
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分,2-丁醇、2-氯丁烷;
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水,洗涤除去其他杂质;
洗涤,再加入CaCl2固体吸水干燥,放置一段时间后过滤.
步骤4:滤液通过蒸馏经进一步精制得产品;
(1)醇和盐酸溶液加热发生取代反应生成卤代烃;
(2)球形冷凝管是用来冷凝回流挥发出的2-丁醇、2-氯丁烷;挥发出的为氯化氢气体,氯化氢气体极易溶于水,吸收需要防倒吸;
(3)卤代烃在强碱溶液中发生水解生成醇,二氯丁烷沸点低易挥发,蒸馏水洗涤除去其中的氢氧化钠溶液;
(4)滤液经进一步精制得产品,精制的操作为蒸馏.
解答 解:(1)醇和盐酸溶液加热发生取代反应生成卤代烃,加入烧瓶的物质中,无水氯化锌是催化剂,
故答案为:无ZnCl2;
(2)球形冷凝管是用来冷凝回流挥发出的2-丁醇、2-氯丁烷;挥发出的为氯化氢气体,氯化氢气体极易溶于水,吸收需要防倒吸,倒扣在烧杯中的漏斗可以起到防倒吸的作用,烧杯中液体为水或氢氧化钠溶液,
故答案为:冷凝回流,提高原料利用率,水或碱溶液;
(3)卤代烃在强碱溶液中发生水解生成醇,二氯丁烷沸点低易挥发,用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,蒸馏水洗涤除去其中的氢氧化钠溶液,第二次用蒸馏水洗涤的目的是蒸馏水洗涤除去其中的氢氧化钠溶液,
故答案为:防止2-氯丁烷水解减少2-氯丁烷挥发;除去残留的氢氧化钠;
(4)滤液经进一步精制得产品,精制的操作为蒸馏,需要c.蒸馏烧瓶d.冷凝管,不需要抽滤操作,所以不需要a.布氏漏斗b.抽滤瓶,
故答案为:ab.
点评 本题考查了有机物的分离提纯实验过程分析,主要是反应原理和实验基本操作的理解应用,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融电解质中,O2-向正极定向移动 | |
| B. | 电池的总反应是:2C4H10+13O2═8CO2+10H2O | |
| C. | 通入空气的一极是正极,电极反应为:O2+4e-+2H2O═4OH- | |
| D. | 通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-═4CO2↑+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当a=b时,c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 当a>b时,c(NH4+)+c(NH3•H2O)>c(Cl-) | |
| C. | 当a<b时,c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 当a与b为任意比时,c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
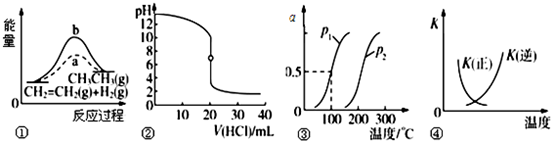
| A. | 图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. | 图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. | 图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)△H,反应CH4的转化率与温度、压强的关系,且P1>P2、△H>0 | |
| D. | 图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0;正、逆反应的平衡常数K随温度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
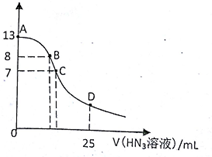
| A. | 水电离出的c(H+):A点小于B点 | |
| B. | 在B点,离子浓度大小为c(OH-)>c(H+)>c(Na+)>c(N3-) | |
| C. | 在C点,滴加的V(HN3)=12.5 mL | |
| D. | 在D点,c(Na+)=2c(HN3)+2 c(N3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | b点对应的溶液中:Al3+、Fe3+、SCN-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:SO32-、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁和钢都属于合金 | |
| B. | 明矾可用作混凝剂去除水中的悬浮物 | |
| C. | 食盐水、稀豆浆、糖水都能产生丁达尔效应 | |
| D. | 以次氯酸钠为有效成分的漂白液可为泳池消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


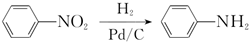
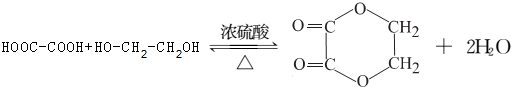 .
.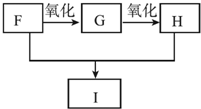
 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com