
| A. | 纳米碳酸钙材料能够产生丁达尔效应 | |
| B. | NOx、SO2、PM2.5颗粒都会导致酸雨 | |
| C. | 纯碱可用于制造玻璃,也可用于除去物品表面的油污 | |
| D. | 糖类、油脂、蛋白质均能发生水解反应 |
分析 A.一种或几种物质分散在另一种物质中所形成的体系称为分散系;
B.PM2.5是造成灰霾天气的“元凶”之一,与酸雨无关;
C.纯碱水解呈碱性,可用于除油污,结合玻璃的成分判断;
D.单糖在催化剂的作用下不能发生水解反应.
解答 解:A.纳米碳酸钙是纯净物,分散系是混合物,故A错误;
B.酸雨是指溶液pH小于5.6的雨水,正常雨水的pH约为5.6,二氧化硫、氮氧化物等物质是形成酸雨的重要物质,二氧化碳排放过多会引起温室效应,不是形成酸雨的气体,PM2.5是造成灰霾天气的“元凶”之一,所以PM2.5颗粒都不会导致酸雨,故B错误;
C.纯碱水解呈碱性,可用于除油污,玻璃的原料有二氧化硅、碳酸钠等,故C正确;
D.糖类中单糖如葡萄糖不能发生水解,故D错误.
故选C.
点评 本题考查较为综合,涉及胶体、酸雨、纯碱以及糖类、油脂、蛋白质的性质等知识,侧重于化学与生产、生活等考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | LiAlH4中H元素的化合价为-1 | |
| B. | LiAlH4L、iAlO2、LiH均是离子化合物 | |
| C. | 1mol LiAlH4在125℃完全分解,转移4mol电子 | |
| D. | 0.5 mol LiAlH4与水充分反应后产生44.8L H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 | |
| B. | X如果是氯化钠,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 | |
| C. | X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 | |
| D. | X如果是氢氧化钠,将碳电极改为铝电极,a和b用导线连接,此时构成原电池铁作负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
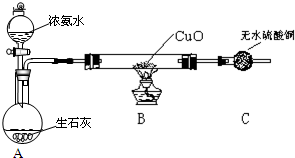
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
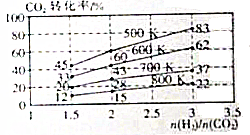 二氧化碳是造成温室效应的主要气体,二氧化碳的回收在利用是减缓温室效应的有效途径之一.
二氧化碳是造成温室效应的主要气体,二氧化碳的回收在利用是减缓温室效应的有效途径之一.| 温度/K CO2转化率/% a/mol | 500 | 600 | 700 | 800 |
| 1.67 | x | 33 | ||
| 1.25 | 60 | 43 | y | |
| 0.83 | z | 32 | w |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应为2CO2+O2+4e-═2CO32- | |
| B. | CO32-向正极移动 | |
| C. | 电子由正极经外电路流向负极 | |
| D. | 电池中CO32-的物质的量将逐渐减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、Al、H2 | B. | F2、K、HCl | C. | NO2、Na、Br2 | D. | HNO3、SO2、H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com