
·ÖĪö ·¢Éś·“Ó¦£ŗ3Cu+8HNO3 =3Cu£ØNO3£©2+4H2O+2NO”ü£¬n£ØCu£©=$\frac{1.92g}{64g/mol}$=0.03mol£¬n£ØHNO3£©=0.5L”Į0.2 mol•L-1=0.1 mol£¬ÓÉ·½³ĢŹ½æÉÖŖCuĶźČ«·“Ó¦£¬øł¾ŻCu¼ĘĖćÉś³ÉNOĪļÖŹµÄĮ攢ĻūŗÄĻõĖįĪļÖŹµÄĮ棬½ų¶ų¼ĘĖćŹ£ÓąĻõĖįĪļÖŹµÄĮ棬ŌŁøł¾ŻV=nVm¼ĘĖćNOĢå»ż£¬øł¾Żc=$\frac{n}{V}$¼ĘĖćĒāĄė×ÓÅØ¶Č£®
½ā“š ½ā£ŗ£ØCu£©=$\frac{1.92g}{64g/mol}$=0.03mol£¬n£ØHNO3£©=0.5L”Į0.2 mol•L-1=0.1 mol£¬
ÓÉ3Cu+8HNO3 =3Cu£ØNO3£©2+4H2O+2NO”üæÉÖŖ£¬Ļ”ĻõĖį¹żĮ棬CuĶźČ«·“Ó¦£¬
£Ø1£©ÉčÉś³ÉµÄŅ»Ńõ»ÆµŖĪļÖŹµÄĮæĪŖx£¬ĻūŗÄHNO3µÄĪļÖŹµÄĮæĪŖy£¬Ōņ£ŗ
3Cu+8HNO3=3Cu£ØNO3£©2+2NO”ü+4H2O
3 8 2
0.03mol y x
£Ø1£©Éś³ÉNOµÄĪļÖŹµÄĮæx=$\frac{0.03mol”Į2}{3}$=0.02mol£¬±ź×¼×“æöĻĀĖłÕ¼µÄĢå»żĪŖ0.02mol”Į22.4L/mol=0.448L£¬
“š£ŗ±ź×¼×“æöĻĀĖłÕ¼µÄĢå»żĪŖ0.448L£»
£Ø2£©ĻūŗÄĻõĖįµÄĪļÖŹµÄĮæy=$\frac{0.03mol”Į8}{3}$=0.08mol£¬Ōņ·“Ó¦ŗóČÜŅŗÖŠH+µÄĪļÖŹµÄĮæÅØ¶ČŹĒ$\frac{0.1mol-0.08mol}{0.5L}$=0.04mol/L£¬
“š£ŗ·“Ó¦ŗóČÜŅŗÖŠH+µÄĪļÖŹµÄĮæÅØ¶ČŹĒ0.04mol/L£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦·½³ĢŹ½µÄ¼ĘĖć£¬Ć÷Č··¢ÉśµÄ·“Ó¦¼“æɽā“š£¬×¢Ņā¶Ō»Æѧ·½³ĢŹ½ŅāŅåĄķ½ā£¬ÕĘĪÕŅŌĪļÖŹµÄĮæĪŖÖŠŠÄµÄ¼ĘĖć£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃéÄæµÄ | ŹµŃé²Ł×÷ | ŹµŃéŌĄķ | |
| A | ŃéÖ¤Fe£ØOH£©3µÄČܽā¶ČŠ”ÓŚMg£ØOH£©2 | ½«FeCl3ČÜŅŗ¼ÓČėMg£ØOH£©2Šü×ĒŅŗÖŠ£¬Õńµ“ | 3Mg£ØOH£©2+2Fe3+?2Fe£ØOH£©3+3Mg2+ |
| B | ÅäÖĘFeCl3ČÜŅŗ | ½«FeCl3¹ĢĢåČܽāÓŚŹŹĮæĮņĖįČÜŅŗ | H+ŅÖÖĘFeCl3Ė®½ā |
| C | ¼ģŃéČÜŅŗÖŠŹĒ·ńŗ¬ÓŠNH4+ | ȔɣĮæŹŌŅŗÓŚŹŌ¹ÜÖŠ£¬¼ÓČėNaOHČÜŅŗ²¢¼ÓČČ£¬ÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃé²śÉśµÄĘųĢå | NH3ČÜÓŚĖ®ŗóČÜÖŹµÄÖ÷ŅŖ“ęŌŚŠĪŹ½ŹĒNH4+”¢OH- |
| D | Ģį“æ»ģÓŠÉŁĮæĻõĖį¼ŲµÄĀČ»ÆÄĘ | ŌŚ½ĻøßĪĀ¶ČĻĀÖʵĆÅØČÜŅŗŌŁĄäČ“½į¾§”¢¹żĀĖ”¢øÉŌļ | ĀČ»ÆÄĘČܽā¶ČĖęĪĀ¶ČÉżøß±ä»Æ²»“󣬶ųĻõĖį¼ŲČܽā¶ČĖęĪĀ¶ČÉżøßĻŌÖųŌö“ó |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCl | B£® | Fe3+ | C£® | 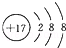 | D£® | CH3COO- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻȵĪ¼ÓĀČĖ®£¬ŌŁµĪ¼ÓKSCNČÜŅŗŗóĻŌŗģÉ« | |
| B£® | ĻȵĪ¼ÓKSCNČÜŅŗ£¬²»ĻŌŗģÉ«£¬ŌŁµĪ¼ÓĀČĖ®ŗóĻŌŗģÉ« | |
| C£® | µĪ¼ÓNaOHČÜŅŗ£¬²śÉś»ŅĀĢÉ«³Įµķ£¬×īŗó³ŹŗģŗÖÉ« | |
| D£® | Ö»ŠčµĪ¼ÓKSCNČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
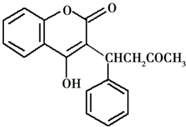
| A£® | ĆšŹóĮéµÄ·Ö×ÓŹ½ĪŖC19H17O4 | |
| B£® | ĆšŹóĮéæÉÓėäåĖ®·¢Éķ¼Ó³É·“Ó¦ | |
| C£® | ·Ö×ÓÖŠĖłÓŠµÄĢ¼Ō×Ó¶¼æÉÄÜŌŚĶ¬Ņ»øöĘ½ĆęÉĻ | |
| D£® | 1 molĆšŹóĮé×ī¶ąæÉÓė8 mol H2 ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Zn”śZn2+ | B£® | H2”śH2O | C£® | Cl2”śCl- | D£® | CuO”śCuCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮæČ”10.08 mL 0.1 mol•L-1 NaHCO3ČÜŅŗÓĆ¼īŹ½µĪ¶Ø¹ÜĮæČ” | |
| B£® | ĪŖ²ā¶ØŠĀÖĘĀČĖ®µÄ pH£¬ÓĆ²£Į§°ōÕŗČ”ŅŗĢåµĪŌŚ pH ŹŌÖ½ÉĻ£¬Óė±ź×¼±ČÉ«æضŌÕÕ¼“æÉ | |
| C£® | Ģ½¾æ“߻ƼĮ¶Ō H2O2·Ö½āĖŁĀŹµÄÓ°Ļģ£ŗŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĻņŅ»Ö§ŹŌ¹ÜÖŠ¼ÓČė2mL 5%H2O2ŗĶ1mL H2O£¬ĻņĮķŅ»Ö§ŹŌ¹ÜÖŠ¼ÓČė2mL 5%H2O2ŗĶ1mL FeCl3ČÜŅŗ£¬¹Ū²ģ²¢±Č½ĻŹµŃéĻÖĻó | |
| D£® | ŅŃÖŖ 4H++4I-+O2=2I2+2H2O£¬ĪŖĮĖĄūÓĆøĆ·“Ó¦Ģ½¾æ·“Ó¦ĖŁĀŹÓėĪĀ¶ČµÄ¹ŲĻµ£¬ĖłÓĆŹŌ¼Į³ż1 mol•L-1 KI ČÜŅŗ”¢0.1 mol•L-1 Ļ”ĮņĖįĶā£¬»¹ŠčŅŖÓƵ½µķ·ŪČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH HCl£¾CH3COOH | |
| B£® | c£ØCl-£©=c£ØCH3COO-£© | |
| C£® | µČĢå»żµÄŃĪĖįŗĶ“×ĖįČÜŅŗ·Ö±šÓė×ćĮæµÄZnĶźČ«·“Ó¦£¬ŃĪĖį²śÉśµÄH2¶ą | |
| D£® | ÓĆĶ¬ÅØ¶ČµÄNaOHČÜŅŗ·Ö±šÓėµČĢå»żµÄŃĪĖįŗĶ“×ĖįČÜŅŗĒ”ŗĆ·“Ó¦ĶźČ«£¬ĻūŗĵÄNaOHČÜŅŗĢå»żŅ»Ńł¶ą |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com