
A.粉碎后的黄铁矿易于向炉中投料 B.粉碎成小颗粒易于燃烧
C.提高黄铁矿的利用率 D.粉碎后杂质易分离
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
A.![]() kg B.
kg B.![]() kg
kg
C.![]() kg D.
kg D.![]() kg
kg
查看答案和解析>>
科目:高中化学 来源: 题型:
A.工业制硝酸:2NaNO3+H2SO4====Na2SO4+2HNO3↑
B.在接触法制硫酸的过程中,用水吸收SO3气体
C.工业合成氨时,将生成的氨液化以提高氨的产率
D.常温下,氮气与氢气难化合,说明N元素的非金属性弱
查看答案和解析>>
科目:高中化学 来源:2013-2014学年吉林省吉林市高三上学期摸底测试化学试卷(解析版) 题型:填空题
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)
 2SO3(g)
△H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g)
△H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
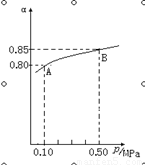
①平衡状态由A到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为 。
该反应的平衡常数为 。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为 ;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com