
分析 碘化钠和氯气反应方程式为2NaI+Cl2=I2+2NaCl,碘在灼烧时会升华,所以灼烧后固体为NaCl,溶液蒸干灼烧前后固体质量减少量为碘与氯元素质量之差,据此分析解答.
解答 解:碘化钠和氯气反应方程式为2NaI+Cl2=I2+2NaCl,碘在灼烧时会升华,所以灼烧后固体为NaCl,溶液蒸干灼烧前后固体质量减少量为碘与氯元素质量之差,设原混合物中NaCl的质量为xg,则NaI的质量为(10-x)g,
2NaI+Cl2=I2+2NaCl 钠盐质量差
300 183
(10-x)g (10-6.34)g
300:183=(10-x)g:(10-6.34)g
x=10-$\frac{(10-6.34)g×300}{183}$=6,
答:原混合物中氯化钠的质量为6g.
点评 本题考查化学方程式的有关计算,为高频考点,明确各个物理量之间关系式是解本题关键,注意差量法的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 对盛在烧杯(敞口)内的氨水加热,氨水中NH${\;}_{4}^{+}$浓度减小 | |
| B. | 对石灰的悬浊液加热使温度升高,悬浊液中Ca(OH)2固体的含量增加 | |
| C. | 高压有利于合成氨的反应 | |
| D. | 500℃左右比室温更有利于合成氨的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇在电池的负极放电生成CO2时,共失去12mol 电子 | |
| B. | 1mol/L碳酸钠溶液中,n(CO32-)+n(HCO3-)+n(H2CO3)=1mol | |
| C. | 25℃时,1L pH=1的醋酸溶液中含有H+的数目小于0.1NA | |
| D. | 电解精炼铜,当电路中转移NA个电子,阳极溶解的铜<32g,阴极析出铜32g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | Cl-Cl | H-Cl |
| 生成(拆开)1mol化学键放出(吸收)的能量 | 436kJ | 243kJ | 431kJ |
| A. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-91.5kJ•mol-1 | |
| B. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=+91.5kJ•mol-1 | |
| C. | H2(g)+Cl2(g)═2HCl(g)△H=-183kJ•mol-1 | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H=+183kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=-2 878 kJ•mol-1 | B. | △H=-2 658 kJ•mol-1 | ||
| C. | △H=-1 746 kJ•mol-1 | D. | △H=-1 526 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
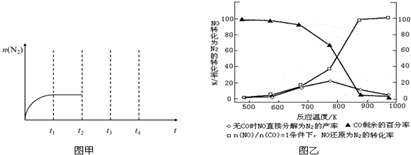
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电源B 极的名称是负极 | |
| B. | 甲装置中电解反应的总化学方程式是:CuSO4+Fe$\frac{\underline{\;电解\;}}{\;}$Cu+FeSO4 | |
| C. | 设电解质溶液过量,则同一时内C、D电极上参加反应的单质或生成的单质的物质的量之比是1:1 | |
| D. | 设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为0.2mol/L. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com