
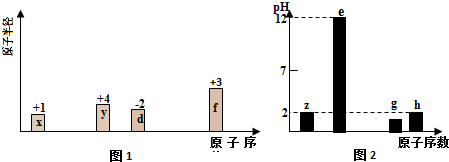
 Q”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£®
Q”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£®·ÖĪö Q”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬ŌņQĪŖCŌŖĖŲ£»XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬ŌņXĪŖOŌŖĖŲ£»RµÄŌ×ÓŠņŹż½éÓŚĢ¼”¢ŃõÖ®¼ä£¬ŌņRĪŖNŌŖĖŲ£»YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ŌņYĪŖAl£»ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£¬ŌņZŌ×ÓĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d54s1£¬ŌņZĪŖCr£®
½ā“š ½ā£ŗQ”¢R”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĒ°ĖÄÖÜĘŚŌŖĖŲ£¬QµÄŅ»ÖÖµ„ÖŹŹĒĢģČ»“ęŌŚµÄ×īÓ²µÄĪļÖŹ£¬ŌņQĪŖCŌŖĖŲ£»XŌ×ÓµÄŗĖĶāµē×ÓÓŠ°ĖÖÖŌĖ¶ÆדĢ¬£¬ŌņXĪŖOŌŖĖŲ£»RµÄŌ×ÓŠņŹż½éÓŚĢ¼”¢ŃõÖ®¼ä£¬ŌņRĪŖNŌŖĖŲ£»YŌŖĖŲµÄĄė×Ó°ė¾¶ŹĒµŚČżÖÜĘŚÖŠ×īŠ”µÄ£¬ŌņYĪŖAl£»ZŹĒµŚĖÄÖÜĘŚÖŠĪ“³É¶Ōµē×Ó×ī¶ąµÄŌ×Ó£¬ŌņZŌ×ÓĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d54s1£¬ŌņZĪŖCr£®
£Ø1£©ZĪŖCrŌŖĖŲ£¬Ō×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ3d54s1£¬¹Ź“š°øĪŖ£ŗ3d54s1£»
£Ø2£©Ķ¬ÖÜĘŚ×Ō×ó¶ųÓŅµēøŗŠŌŌö“ó£¬Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀµēøŗŠŌ¼õŠ”£¬¹ŹµēøŗŠŌ£ŗO£¾N£¾C£¾Al£¬
¹Ź“š°øĪŖ£ŗO£¾N£¾C£¾Al£»
£Ø3£©NCl3·Ö×ÓNŌ×ÓŠĪ³É3øöN-Cl¼ü£¬ŗ¬ÓŠ1¶Ō¹Ā¶Ōµē×Ó£¬ŌӻƹģµĄŹżÄæĪŖ4£¬NŌ×Ó²ÉČ”sp3Ōӻƣ¬NŌ×ÓµÄ×īĶā²ćÖ»ÓŠ2s”¢2p¹²4¹Ź¹ģµĄ£¬Ć»ÓŠd¹ģµĄ£¬ĪŽ·ØŠĪ³ÉNCl5£¬
¹Ź“š°øĪŖ£ŗsp3£»NŌ×ÓµÄ×īĶā²ćÖ»ÓŠ2s”¢2p¹²4¹Ź¹ģµĄ£¬Ć»ÓŠd¹ģµĄ£¬ĪŽ·ØŠĪ³ÉNCl5£»
£Ø4£©ÅäŗĻĪļ¼×µÄ·Ö×ÓŹ½ĪŖCrCl3•4H2O£¬ÅäĪ»ŹżĪŖ6£®Č”1mol¼×ČÜÓŚĖ®£¬¼ÓČė×ćĮæµÄAgNO3ČÜŅŗ£¬µĆµ½143.5g°×É«³ĮµķĪŖAgCl£¬ĘäĪļÖŹµÄĮæĪŖ1mol£¬ŌņÓŠ1øöCl-“¦ÓŚĶā½ē£¬2øöCl-“¦ÓŚÄŚ½ē£¬Ōņ¼×µÄ»Æ½į¹¹¼ņŹ½ĪŖ£ŗ[Cr£ØH2O£©4Cl2]Cl£¬ŌŚĖįŠŌČÜŅŗÖŠ£¬¼×·¢ÉśĖ®ŗĻ·“Ó¦×Ŗ»ÆĪŖŅŅ£ØZCl3•6H2O£©£¬ŅŅµÄÅäĪ»Ō×ÓÖ»ÓŠŅ»ÖÖ£¬ÅäĪ»ŹżĪŖ6£¬ŌņŅŅĪŖ[Cr£ØH2O£©6]Cl3£¬¼×”śŅŅµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ[Cr£ØH2O£©4Cl2]Cl+2H2O$\frac{\underline{\;H+\;}}{\;}$[Cr£ØH2O£©6]Cl3 £¬
¹Ź“š°øĪŖ£ŗ[Cr£ØH2O£©4Cl2]Cl£»[Cr£ØH2O£©4Cl2]Cl+2H2O$\frac{\underline{\;H+\;}}{\;}$[Cr£ØH2O£©6]Cl3 £»
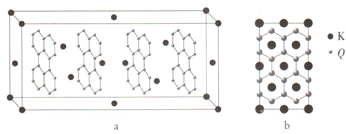
£Ø5£©¾§°ūÖŠKŌ×ÓŹżÄæĪŖ4+8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=8£¬CŌ×ÓŹżÄæĪŖ12”Į4+8”Į$\frac{1}{2}$”Į4=64£¬K”¢CŌ×ÓŹżÄæÖ®±ČĪŖ8£ŗ64=1£ŗ8£¬¹ŹøĆ²å²ć»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒKC8£¬
¹Ź“š°øĪŖ£ŗKC8£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹ÓėŠŌÖŹµÄ漲飬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢µēøŗŠŌ”¢ŌӻƷ¢Éś”¢ÅäŗĻĪļ”¢¾§°ū¼ĘĖćµČ£¬£Ø4£©×¢ŅāÄŚ½ēÓėĶā½ē²»Ķ¬£¬£Ø5£©ŠčŅŖѧɜ¾ß±øŅ»¶ØµÄæÕ¼äĻėĻ󣬽įŗĻ¾łĢƷؼĘĖć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾Ū±ūĻ©µÄĮ“½ŚŹĒ-CH2-CH2-CH2- | |
| B£® | Ļņ±½·ÓČÜŅŗÖŠµĪ¼ÓNa2CO3ČÜŅŗ£ŗ2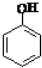 +CO${\;}_{3}^{2-}$”ś +CO${\;}_{3}^{2-}$”ś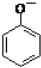 +CO2”ü+H2O +CO2”ü+H2O | |
| C£® | 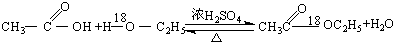 | |
| D£® | ±½µÄĶ¬ĻµĪļÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬ĖµĆ÷Ģž»ł¶Ō±½»·µÄŠŌÖŹ²śÉśĮĖ½Ļ“óµÄÓ°Ļģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŹŅĪĀŹ±£¬Ļņ100mL 0.1mol/L NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1mol/L NaOHČÜŅŗ£¬µĆµ½ČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£®
ŹŅĪĀŹ±£¬Ļņ100mL 0.1mol/L NH4HSO4ČÜŅŗÖŠµĪ¼Ó0.1mol/L NaOHČÜŅŗ£¬µĆµ½ČÜŅŗpHÓėNaOHČÜŅŗĢå»żµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
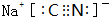 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µķ·Ū | B£® | ÕįĢĒ | C£® | ¹ūĢĒ | D£® | ĀóŃæĢĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com