
| A. | ①③⑤⑦⑨ | B. | ②④⑥⑧⑩ | C. | ②⑦⑧⑩ | D. | ②⑤⑧⑩ |
分析 ①碳酸钠、碳酸氢钠溶液中含有离子种类相同;
②碳酸氢钠溶液中碳酸氢根离子浓度较大,碳酸钠溶液中碳酸根离子浓度较大,则A、B两种溶液中各种离子的浓度不相同;
③碳酸根离子的水解程度大于碳酸氢根离子,水解程度越强,则水电离出的氢离子数目越多;
④碳酸钠溶液中离子浓度大小为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),碳酸氢钠溶液中离子浓度大小为c (Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),据此进行判断;
⑤根据电荷守恒及碳酸钠、碳酸氢钠的水解程度大小判断;
⑥根据碳酸钠、碳酸氢钠溶液的电荷守恒判断;
⑦碳酸氢钠溶液中HCO3-的水解程度大于其电离程度,据此判断c(CO32-)、c(H2CO3)的浓度大小;
⑧根据碳酸钠、碳酸氢钠溶液中的质子守恒分析;
⑨碳酸钠的第一步水解程度大于第二步;
⑩根据碳酸钠、碳酸氢钠的物料守恒分析.
解答 解:①NaHCO3、Na2CO3溶液存在的粒子为:Na+、H+、HCO3-、CO32-、OH-,所以两种溶液中离子种类相同,所以A、B两种溶液中所含离子种类相同,故①正确;
②由于盐的水解程度较小,碳酸钠、碳酸氢钠两种溶液中各种离子的浓度不相同,如:碳酸氢钠溶液中碳酸氢根离子浓度较大,碳酸钠溶液中碳酸根离子浓度较大,故②错误;
③由于碳酸根离子的水解程度大于碳酸氢根离子,则碳酸钠溶液中水电离出的H+个数大于碳酸氢钠,即:B>A,故③正确;
④碳酸钠溶液中离子浓度大小为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),碳酸氢钠溶液中离子浓度大小为:c (Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-),A、B两种溶液中各种离子浓度由大到小顺序不相同,故④正确;
⑤根据电荷守恒可知,溶液中阴离子的物质的量浓度之和=c(Na+)+c(H+),钠离子浓度相同,由于A中氢氧根离子浓度小于B,则A中c(H+)大于B,则溶液中阴离子的物质的量浓度之和A>B,故⑤错误;
⑥A、B两种溶液中离子的电荷守恒式都是:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),故⑥正确;
⑦碳酸氢钠溶液中,HCO3-的水解程度大于其电离程度,则A溶液中:c(CO32-)>c(H2CO3),故⑦正确;
⑧碳酸钠中的质子守恒为:c(H+)+2c(H2CO3)+c(HCO3-)=c(OH-),碳酸氢钠溶液中的质子守恒为:c(H+)+c(H2CO3)=c(OH-)+c(CO32-),所以A、B两种溶液中离子的质子守恒式不相同,故⑧错误;
⑨碳酸钠溶液中,其第一步水解程度大于第二步,则B溶液中:c(HCO3-)>c(H2CO3),故⑨正确;
⑩碳酸钠溶液中的物料守恒为:c(Na+)=2c(H2CO3)+2c(HCO3-)+2c(CO32-),碳酸氢钠溶液中的物料守恒为:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-),所以A、B两种溶液中离子的物料守恒式不相同,故⑩错误;
所以不正确的为:②⑤⑧⑩,
故选D.
点评 本题考查了离子浓度大小比较,题目难度中等,明确物料守恒、电荷守恒、质子守恒的含义为解答关键,注意熟练掌握盐的水解原理及其影响因素,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及灵活应用能力.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | C2H4 | B. | C2H6 | C. | C3H6 | D. | C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,5v正(O2)=4v逆(NO) | |
| B. | 若单位时间内生成nmol NO的同时,生成nmol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 | |
| D. | 化学反应速率关系是:2v正(NH3)=3v正(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①②③ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.
向电解质溶液中加入新物质时,其导电性符合如图所示变化趋势的实验操作是②.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子的数目相等 | B. | 粒子的总的物质的量相等 | ||
| C. | 正电荷总数和负电荷总数应相等 | D. | 反应前后原子的数目不一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2与D2、T2互为同位素 | |
| B. | 氯化钠溶液和氢氧化铁胶体可以用过滤的方法分离 | |
| C. | NH3溶于水可以导电,但不是电解质 | |
| D. | SO2、NO2均属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
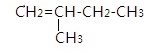 、
、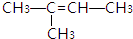 、
、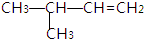 烯烃的名称:
烯烃的名称:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com