
【题目】用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 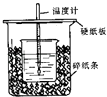
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 .
(2)烧杯间填满碎纸条的作用是 .
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等、不相等”),所求中和热(填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”).
【答案】
(1)环形玻璃搅拌棒
(2)减少实验过程中的热量损失
(3)偏小
(4)不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关
(5)偏小
【解析】解:(1)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故答案为:环形玻璃搅拌器;(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是:减少实验过程中的热量损失,故答案为:减少实验过程中的热量损失;(3)大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,故答案为:偏小;(4)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25molL﹣1H2SO4溶液跟50mL0.55molL﹣1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所测得中和热数值相等,
故答案为:不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关;(5)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ,故答案为:偏小.
(1)根据量热计的构造来判断该装置的缺少仪器;(2)中和热测定实验成败的关键是保温工作;(3)不盖硬纸板,会有一部分热量散失;(4)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;(5)根据弱电解质电离吸热分析.


科目:高中化学 来源: 题型:
【题目】下列有关气体摩尔体积的描述中正确的是( )
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 通常状况(室温、101kP)下,气体摩尔体积约为22.4 L/mol
C. 标准状况(0℃、101kP)下,气体摩尔体积约为22.4 L
D. 标准状况(0℃、101kP)下,1 mol H2O的体积是22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D反应中,表示该反应速率最快的是( )
A.v(A)=0.5 molL﹣1s﹣1
B.v(B)=0.3 molL﹣1s﹣1
C.v(C)=0.8 molL﹣1s﹣1
D.v(D)=1.6 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置制取NH3,并用AlCl3溶液吸收多余NH3制Al(OH)3,最后回收NH4Cl,能达到实验目的的是

A. 用装置甲制取NH3
B. 用装置乙吸收NH3制取Al(OH)3
C. 用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌
D. 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A、B的分子式均为C11H12O5 , 均能发生如下变化.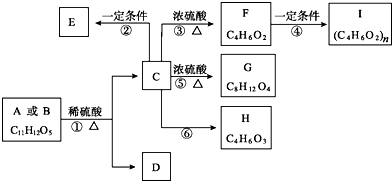
已知:
①A、B、C、D均能与NaHCO3反应;
②只有A、D能与FeCl3溶液发生显色反应,A苯环上的一溴代物只有两种;
③F能使溴水褪色且不含有甲基;
④H能发生银镜反应.
根据题意回答下列问题:
(1)反应③的反应类型是;反应⑥的条件是 .
(2)写出F的结构简式;D中含氧官能团的名称是 .
(3)E是C的缩聚产物,写出反应②的化学方程式 .
(4)下列关于A~I的说法中正确的是(选填编号).a.I的结构简式为 ![]() b.D在一定条件下也可以反应形成高聚物
b.D在一定条件下也可以反应形成高聚物
c.G具有8元环状结构 d.等质量的A与B分别与足量NaOH溶液反应,消耗等量的NaOH
(5)写出B与足量NaOH溶液共热的化学方程式 .
(6)D的同分异构体有很多种,写出同时满足下列要求的其中一种同分异构体的结构简式 . ①能与FeCl3溶液发生显色反应
②能发生银镜反应但不能水解
③苯环上的一卤代物只有2种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种只含Al、Fe、Cu的合金,称取a g样品,设计下列实验流程分析该合金的组成 
下列相关叙述正确的是( )
A.若向溶液F中加入K4[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液F中含有Fe2+
B.溶液N为深蓝色,说明溶液N中含大量Cu2+
C.合金样品中Cu的质量分数为 ![]() ×100%
×100%
D.合金样品中Al的质量分数为 ![]() ×100%
×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作均要用到玻璃棒:①过滤;②蒸发;③溶解;④向容量瓶里转移液体,其中玻璃棒的作用相同的是
A. ①和②B. ①和③C. ③和④D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种可溶性物质甲、乙、丙、丁、戊,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Al3+、Cu2+、Ba2+、Fe3+和五种阴离子Cl﹣、OH﹣、NO ![]() 、CO
、CO ![]() 、X中的一种.
、X中的一种.
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是和 . (填化学式)
(2)物质丙中含有离子X.为了确定X,现将(1)中的两种物质记为甲和乙,当丙与甲的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀硝酸,沉淀部分溶解,剩余白色固体,则物质丙为 . (填化学式)
(3)将19.2g Cu投入装有足量丁溶液的试管中,Cu不溶解,再滴加稀硫酸,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式 , 若要将Cu完全溶解,至少加入硫酸的物质的量是 .
(4)戊溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,某有机物和过量Na反应得到V1L氢气,另一份等量的该有机物和足量的NaHCO3反应得到V2L二氧化碳,若V1=V2≠0,则该有机物可能是( )
A.![]()
B.HOOC﹣COOH
C.HOCH2CH2OH
D.CH3COOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com