
硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
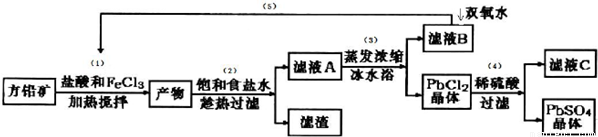
已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2C1-(aq) PbCl42-(aq)△H>0
PbCl42-(aq)△H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9和7.
(I )流程中加入盐酸可以控制溶液的pH<1.9,主要目的是___________,反应过程中可观察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为___________;
(II) 步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________(请用平衡移动原理解释)
(III )上述流程中可循环利用的物质有___________;
(IV)炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染.水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-。各形态的铅浓度分数α与溶液pH 变化的关系如图所示:
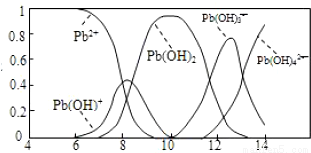
①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH,溶液变浑浊,继续滴加NaOH溶液又变澄清;pH≥13时,溶液中发生的主要反应的离子方程式为___________;
②除去溶液中的Pb2+:科研小组用一种新型试剂可去除水中的痕量铅和其他杂质离子,实验结果记录如下:
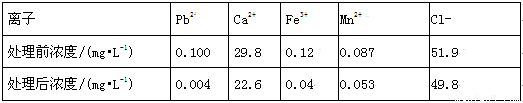
Ⅰ.新型试剂处理后的水中Pb2+浓度转化率为___________;
Ⅱ.若新型试剂(DH)在脱铅过程中主要发生的反应为:2DH(s)+Pb2+ D2Pb(s)+2H+,则脱铅时最合适的pH约为___________
D2Pb(s)+2H+,则脱铅时最合适的pH约为___________
A.4 B.6 C. 10 D. 12
科目:高中化学 来源:2015-2016学年江西省等四校高一下第二次月考化学试卷(解析版) 题型:填空题
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。回答下列问题:
(1) Y在元素周期表中的位置为_____________________________.
(2) 上述元素的最高价氧化物对应的水化物酸性最强的是_____________________ (写化学式),非金属气态氢化物还原性最强的是_______________(写化学式)。
(3) Y、G的单质或两元素之间形成的化合物可作水消毒剂的有__________________ (写出其中两种物质的化学式))。
(4) ZX的电子式为_________________;ZX与水反应放出气体的化学方程式为__________________。
(5) 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),放电时,电池的正极反应

查看答案和解析>>
科目:高中化学 来源:2016届云南省高三下学期第八次月考理综化学试卷(解析版) 题型:填空题
新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为______,该能层具有的原子轨道数为_______。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是_________,B原子的杂化轨道类型是________。
Li、B、H元素的电负性由大到小排列顺序为________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径Li+_______H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:

M是________ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为________,NaH的理论密度是___________g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一卷理综化学试卷(解析版) 题型:实验题
硫酸铅,又名石灰浆,可用于铅蓄电池、纤维增重剂、涂料分析试剂。工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
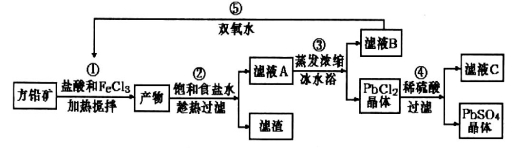
已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5。
②PbCl2(s)+2C1-(aq) PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9和7。
(1)流程中加入盐酸可以控制溶液的pH<1.9,主要目的是__________________________。
反应过程中可观察到淡黄色沉淀,则①对应的离子方程式为_____________________。
(2)②所得的滤液A蒸发浓缩后再用冰水浴的目的是_____(请用平衡移动原理解释)
(3)④中对应反应的平衡常数表达式________。
(4)上述流程中可循环利用的物质有_________________。
(5)炼铅和用铅都会使水体因重金属铅的含量增大而造成严重污染。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-。各形态的铅浓度分数x与溶液pH变化的关系如图所示:
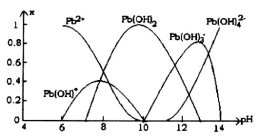
①探究Pb2+的性质:向含Pb2+的溶液中逐滴滴加NaOH,溶液变浑浊,继续滴加NaOH溶液又变澄清;pH≥13时,溶液中发生的主要反应的离子方程式为_________________.。
②除去溶液中的Pb2+:科研小组用一种新型试剂可去除水中的痕量铅和其他杂质离子,
实验结果记录如下:
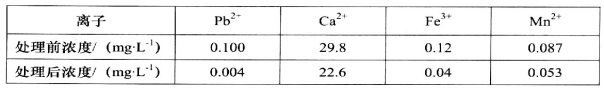
I.由表可知该试剂去除Pb2+的效果最好,请结合表中有关数据说明去除Pb2+比Fe3+效果好的理由是_____。
Ⅱ.若新型试剂(DH)在脱铅过程中主要发生的反应为:2DH(s)+Pb2+?D2Pb(s)+2H+,则脱铅时最合适的pH约为________。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一卷理综化学试卷(解析版) 题型:选择题
民以食为天,食品安全越来越受到大家的关注。下列有关说法正确的是
A.二氧化硫有毒,严禁将其添加到任何食品和饮料中
B.饮食“镉大米”会影响骨骼和肾脏,镉元素属于重金属元素
C.使用增塑剂——邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶
D.面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2
查看答案和解析>>
科目:高中化学 来源:2016届陕西西藏民族学院附中高三下考前三模理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是()
A. 1mol铁与1molCl2充分反应,转移电子数为3NA
B.常温常压下,2gD216O中含中子数、质子数、电子数均不相等
C. 14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
D.在含A13+总数为NA的AlC13溶液中,Cl-总数为3NA
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮复习训练六化学试卷(解析版) 题型:实验题
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等.某化学兴趣小组用模拟制备氨基甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g) NH2COONH4(s)△H<0
NH2COONH4(s)△H<0
(1)制备氨基甲酸铵的装置如图1所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。
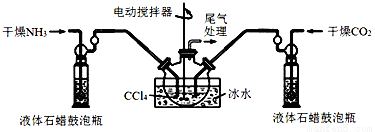
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是__________________,液体石蜡鼓泡瓶的作用是_____________;
②从反应后的混合物中分离出产品的实验方法是_____________(填写操作名称),为了得到干燥产品,应采取的方法是_____________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
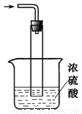
③尾气处理装置如图所示,能否将浓H2SO4改为稀H2SO4_____________(填“能”或“否”),理由是_____;
(2)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.570g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000g.则样品中氨基甲酸铵的质量分数为_____________。[Mr(NH2COONH4)=78、Mr(NH4HCO3)=79、Mr(CaCO3)=100].
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前周练模拟化学试卷(解析版) 题型:选择题
一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是

A.B极中填充多孔的炭或石墨毡,目的是为了增加导电性
B.电池放电时,A极电极反应为:2Na++xS+2e-=Na2SX
C.电池放电时,Na+向电极A极移动
D.电池放电的总反应为2Na+xS=Na2SX,每消耗1molNa转移2mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏育才中学孔德校区高一下6月考化学卷(解析版) 题型:选择题
下列反应中,与其它三个反应不属于同一类型的反应是( )
A.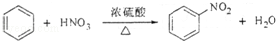
B.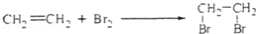
C.CH3CH2OH +CH3COOH
+CH3COOH CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.CH4+Cl2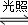 CH3Cl+HCl
CH3Cl+HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com