
| A. | NaOH | B. | AlCl3 | C. | K2S | D. | Cl2 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,含有离子键的化合物为离子化合物,离子化合物中可能含有共价键,只含共价键的化合物为共价化合物.
解答 解:A.NaOH的电子式: ,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,属于含有共价键的离子化合物,故A正确;
,氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,属于含有共价键的离子化合物,故A正确;
B.AlCl3在气态时是双聚分子,结构式为: ,只含共价键,是共价化合物,故B错误;
,只含共价键,是共价化合物,故B错误;
C.K2S的电子式: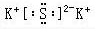 ,只含离子键,属于离子化合物,不含共价键,故C错误;
,只含离子键,属于离子化合物,不含共价键,故C错误;
D. 是单质,只含共价键,故D错误;
是单质,只含共价键,故D错误;
故选A.
点评 本题考查了化合物和化学键的关系,明确基本概念是解本题关键,根据化合物中存在的化学键来分析解答,易错选项是B,AlCl3在气态时是双聚分子只含共价键,为易错点,题目难度不大.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:解答题
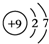 ,五种元素原子半径从大到小的顺序是Na、Si、O、F、H(填元素符号);
,五种元素原子半径从大到小的顺序是Na、Si、O、F、H(填元素符号); ,ED4的电子式是
,ED4的电子式是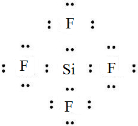 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
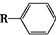 $→_{一定条件}^{CO,HCl}$
$→_{一定条件}^{CO,HCl}$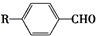 ,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径:
,为合成某种液晶材料的中间体M,有人提出如下不同的合成途径: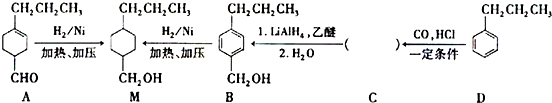
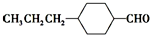 和
和 (写结构简式)生成.
(写结构简式)生成.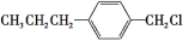 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
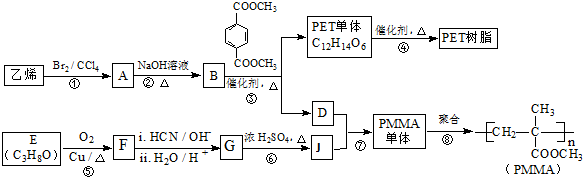 已知:
已知: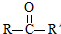 $→_{ii.H_{2}O/H+}^{i.HCN/OH-}$
$→_{ii.H_{2}O/H+}^{i.HCN/OH-}$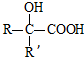 (R、R’代表烃基)
(R、R’代表烃基) .
. .
. .
.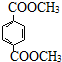 与足量NaOH溶液反应时,最多消耗4mol NaOH
与足量NaOH溶液反应时,最多消耗4mol NaOH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀盐酸反应:Zn+2H+=Zn2++H2↑ | |
| B. | 溴化钠溶液与氯气反应:Br-+Cl2=Cl-+Br2 | |
| C. | 氢氧化铜与稀硫酸反应:OH-+H+=H2O | |
| D. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、Na+、Cl-、SCN- | B. | Na+、Cu2+、NO3-、Cl- | ||
| C. | Na+、H+、NO3-、SO42- | D. | Al3+、Na+、Cl-、NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:O2->Na+>Mg2+>Al3+>F- | |
| B. | 热稳定性:HCl>H2S>PH3>AsH3 | |
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4<H2SO4 | |
| D. | 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
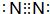 ;B的原子在周期表中的位置是第三周期ⅡA族
;B的原子在周期表中的位置是第三周期ⅡA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com