
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10mL浓度为0.1mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.![]() 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-)
【答案】D
【解析】
A.酸溶液、碱溶液抑制了水的电离,溶液显示中性前,随着氨水的加入,溶液中氢离子浓度逐渐减小,水的电离程度逐渐增大;当氨水过量后,随着溶液中氢氧根离子浓度逐渐增大,水的电离程度逐渐减小,所以滴加过程中,水的电离程度先增大后减小,故A错误;
B.由CH3COONH4的水解常数Kh=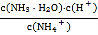 ,随着氨水的加入,c(H+)逐渐减小,Kh不变,则
,随着氨水的加入,c(H+)逐渐减小,Kh不变,则![]() 始终减小,故B错误;
始终减小,故B错误;
C.n(CH3COOH)与n(CH3COO-)之和为0.001mol,始终保持不变,由于溶液体积逐渐增大,所以c(CH3COOH)与c(CH3COO-)之和逐渐减小,故C错误;
D.当加入氨水的体积为10mL时,醋酸和一水合氨的物质的量相等,由于二者的电离常数相等,所以溶液显示中性,c(H+)=c(OH-),根据电荷守恒可知:c(NH4+)=c(CH3COO-),故D正确;
故答案为D。


科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式正确的是( )
A.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:Na2S2O3+2H+=SO2↑+S↓+2Na++H2O
B.硝酸铁溶液中加入少量碘化氢:2Fe3++2I-=2Fe2++I2
C.向NaClO溶液中通入少量CO2制取次氯酸:ClO-+H2O+CO2=HClO+HCO3-
D.硫酸铝铵与氢氧化钡以1:2混合形成的溶液:Al3++2SO42-+2Ba2++4OH-=BaSO4↓+AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是符合绿色化学理念的新型发电装置。如图为氢氧燃料电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b表示)。
(2)负极反应式为___,正极反应式为___。
(3)用该燃料电池作电源,用Pt作电极电解饱和食盐水:
①写出阴极的电极反应式:___。
②写出总反应的离子方程式:___。
③当阳极产生7.1gCl2时,燃料电池中消耗标况下H2___L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用CO2来制备清洁液体颜料甲醇,有关化学反应如下:
反应Ⅰ:CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1=﹣49.6kJmol-1
反应Ⅱ:CO2(g)+H2(g)H2O(g)+CO(g) △H2=+41kJmol-1
(1)反应Ⅰ在___(填“低温”或“高温”)下可自发反应。
(2)有利于提高上述反应甲醇平衡产率的条件是___。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(3)在Cu﹣ZnO/ZrO2催化下,CO2和H2混合气体,体积比1:3,总物质的量amol进行反应,测得CO2转化率、CH3OH和CO选择性随温度、压强变化情况分别如图所示(选择性:转化的CO2中生成CH3OH或CO的百分比)。

①下列说法正确的是___。
A.压强可影响产物的选择性
B.CO2平衡转化率随温度升高先增大后减小
C.由图1可知,反应的最佳温度为220℃左右
D.及时分离出甲醇和水以及使氢气和二氧化碳循环使用,可提高原料利用率
②250℃时,反应Ⅰ和Ⅱ达到平衡,平衡时容器体积为VL,CO2转化率为25%,CH3OH和CO选择性均为50%,则该温度下反应Ⅱ的平衡常数为___。
③分析图2中CO选择性下降的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物C是一种药物的中间体,其合成路线如下图所示:
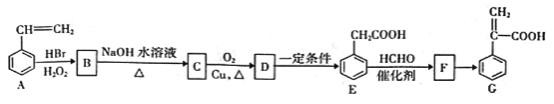
已知:①CH3CH=CH2+HBr![]() CH3CH2CH2Br
CH3CH2CH2Br
②CH3COOH+HCHO![]() HOCH2CH2COOH
HOCH2CH2COOH
回答下列问题:
(1)F中含氧官能团的名称为_______。
(2)C→D的化学方程式为_______。
(3)D→E、E→F的反应类型分别为_______、_______;F→G的反应条件为_______。
(4)下列说法正确的是_______(填标号)。
a. A中所有原子可能都在同一平面上
b. B能发生取代、加成、消去、缩聚等反应
c.合成路线中所涉及的有机物均为芳香族化合物
d.一定条件下1mol有机物G最多能与4molH2发生反应
(5)化合物F有多种同分异构体,其中同时满足下列条件的同分异构体的结构简式为应_______。
① 属于芳香族化合物,且含有两个甲基;
② 能发生水解反应和银镜反应;
③ 能与FeCl3发生显色反应;
④ 核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1。
(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻对位。根据题中的信息,以甲苯为原料合成有机物![]() ,请设计合成路线:_______(无机试剂及溶剂任选)。合成路线流程图示例如下:
,请设计合成路线:_______(无机试剂及溶剂任选)。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() 的
的![]() ,下列说法正确的是
,下列说法正确的是
A.升高温度,正向反应速率增加,逆向反应速率减小
B.达到平衡后,升温或增大压强都有利于该反应平衡正向移动
C.升高温度有利于反应速率增加,从而缩短达到平衡的时间
D.达到平衡后,降温或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
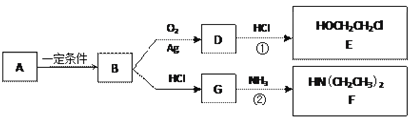
(1)B的结构简式是_________________
(2)A可能属于下列哪类物质___________
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是___________。
反应②可表示为:G + NH3→ F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示): ____________________________________
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知:![]() )
)
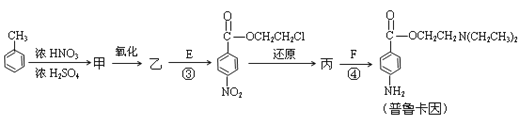
(4)甲的结构简式是 _________________。
由甲苯生成甲的反应类型是_________________。
(5)乙中有两种含氧官能团,反应③的化学方程式是___________________________________
(6)丙中官能团的名称是_______________________________________。
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是_____________________。
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是__________________________________________。
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,电化学原理与微生物工艺相组合的电解脱硝法,可除去引起水华的NO3-原理是将NO3-还原为N2。下列说法正确的是( )
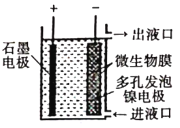
A. 若加人的是![]() 溶液,则导出的溶液呈碱性
溶液,则导出的溶液呈碱性
B. 镍电极上的电极反应式为:![]()
C. 电子由石墨电极流出,经溶液流向镍电极
D. 若阳极生成![]() 气体,理论上可除去
气体,理论上可除去![]() mol
mol![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
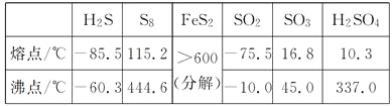
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为____________________________,基态S原子电子占据最高能级的电子云轮廓图为________形。
(2)根据价层电子对互斥理论,H2S、SO2、SO3的气态分子中,中心原子价层电子对数不同于其他分子的是__。
(3)图(a)为S8的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为__________________。
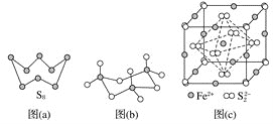
(4)气态三氧化硫以单分子形式存在,其分子的立体构型为________形,其中共价键的类型有________种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为________。
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为anm、FeS2相对式量为M、阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______________________________g·cm-3;晶胞中Fe2+位于![]() 所形成的正八面体的体心,该正八面体的边长为________nm。
所形成的正八面体的体心,该正八面体的边长为________nm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com