
【题目】“电解质的溶液中所有阳离子所带的正电荷数与所有阴离子所带的负电荷数相等,故显电中性,常称电荷守恒”.某盐的溶液中含有Na+、Mg2+、Cl﹣、SO ![]() 四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO
四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl﹣ 为0.4mol,则SO ![]() 物质的量为( )
物质的量为( )
A.0.1mol
B.0.3mol
C.0.5mol
D.0.15mol
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。 设起始
CO(g)+3H2(g)。 设起始![]() ,在恒压下,平衡时CH4的体积分数
,在恒压下,平衡时CH4的体积分数![]() 与Z和T(温度)的关系如图所示,下列说法错误的是
与Z和T(温度)的关系如图所示,下列说法错误的是
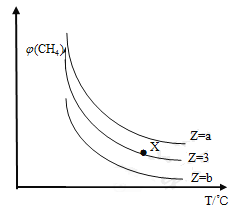
A. 该反应的焓变△H>0
B. 图中Z的大小为b>3>a
C. 图中X点对应的平衡混合物中![]()
D. 温度不变时,加压,平衡逆向移动,甲烷的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《中华人民共和国食品安全法》于2009年6月1日起实施。下列做法不利于食品安全的是:
A.用聚氯乙烯塑料袋包装食品
B.在食用盐中添加适量的碘酸钾
C.在食品加工中科学使用食品添加剂
D.研发高效低毒的农药,降低蔬菜的农药残留量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写下列空格
(1)同温同压下,有0.3molO2与0.2molO3 , 它们的质量之比为 , 它们所含的原子数之比为 , 它们的体积之比为 , 它们的密度之比为 .
(2)由 ![]() H和
H和 ![]() O构成的水摩尔质量为 , 10g该水分子的物质的量为 , 含中子mol.
O构成的水摩尔质量为 , 10g该水分子的物质的量为 , 含中子mol.
(3)实验室需要0.1molL﹣1 NaOH溶液480mL.根据溶液的配制情况回答下列问题:根据计算用托盘天平称取NaOH的质量为g.在实验中其他操作均正确,若定容时俯视刻度线,则所得溶液浓度0.1molL﹣1(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度0.1molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g铁投入200mL某浓度的盐酸中,铁和盐酸恰好完全反应.求:
(1)11.2g铁的物质的量
(2)所用盐酸中HCl的物质的量浓度
(3)反应中生成的H2在标准状况下的体积.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗盐中含有Ca2+、Mg2+及SO ![]() ,除去杂质离子所加入的试剂及顺序可以是:试剂①NaOH、试剂②、试剂③、试剂④ . 在加试剂③后,应先进行一个实验操作之后再加入试剂④.
,除去杂质离子所加入的试剂及顺序可以是:试剂①NaOH、试剂②、试剂③、试剂④ . 在加试剂③后,应先进行一个实验操作之后再加入试剂④.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为__.
(2)表中元素原子半径最大的是(写元素符号)__.
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__.
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y 单质比1mol S 得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1mol X 的最高价化合物,恢复至室温,放热687kJ.已知该化合物的熔沸点分别为﹣69℃和58℃,写出该反应的热化学方程式:__.
(5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中的两种元素组成,气体的相对分子质量都小于50.为防止污染,将生成的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH 溶液和1mol O2,则两种气体的分子式分别为__,物质的量分别为__,生成硫酸铜物质的量为__.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com