
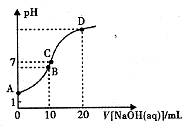
 常温下,用0.1 mol/LNaOH溶液滴定10mL 0.1mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法不正确的是( )
常温下,用0.1 mol/LNaOH溶液滴定10mL 0.1mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法不正确的是( )| A. | A点溶液中加入少量水:$\frac{c(O{H}^{-})}{c({H}_{2}A)}$增大 | |
| B. | B点:c( HA -)>c(H+)>c(A2一)>c(H2A) | |
| C. | C点:c(Na+)=c(HA-)+2c( A2-) | |
| D. | 水电离出来的c(OH-):B点>D点 |
分析 A.A点为H2A溶液,0.1mol/L的H2A溶液的pH大于1,说明H2A为弱酸,稀释后氢离子、H2A的浓度减小,而氢氧根离子浓度增大;
B.B点加入10mL氢氧化钠溶液,反应后溶质为NaHA,溶液的pH小于7,说明HA-的电离程度大于其水解程度,则c(A2-)>c(H2A)结合氢离子厉害来自水的电离判断,
C.C点溶液的pH=7,则c(H+)=c(OH-),结合电荷守恒判断;
D.B点HA-的电离程度大于其水解程度,溶液呈酸性,抑制了水的电离,而D点恰好反应生成Na2A,A2-水解促进了水的电离.
解答 解:A.根据图象可知,0.1mol/L的H2A溶液的pH大于1,说明H2A为弱酸,若A点溶液中加入少量水,溶液中氢离子、H2A的浓度减小,由于水的离子积不变,则氢氧根离子浓度增大,所以$\frac{c(O{H}^{-})}{c({H}_{2}A)}$的比值增大,故A正确;
B.B点时加入了10mLNaOH溶液,反应后溶质为NaHA,此时溶液的pH小于7,说明HA-的电离程度大于其水解程度,则c(A2-)>c(H2A),由于氢离子还来自水的电离,则c(H+)>c(A2-),溶液中离子浓度大小为:c( HA -)>c(H+)>c(A2-)>c(H2A),故B正确;
C.C点溶液的pH=7,为中性溶液,则c(H+)=c(OH-),根据电荷守恒c(Na+)+c(H+)=c(HA-)+2c( A2-)+c(OH-)可知:c(Na+)=c(HA-)+2c( A2-),故C正确;
D.B点反应后溶质为NaHA,HA-的电离程度大于其水解程度,溶液呈酸性,氢离子抑制了水的电离,而D点加入20mL氢氧化钠溶液,二者恰好反应生成Na2A,A2-水解促进了水的电离,所以水电离的c(OH-):B点<D点,故D错误;
故选D.
点评 本题考查了离子浓度大小比较、溶液酸碱性与溶液pH的计算,题目难度中等,明确图象曲线对应溶质为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、SO32-、S2-、K+ | B. | Fe3+、Cl-、S2-、Ba2+ | ||
| C. | Cu2+、Cl-、S2-、K+ | D. | Na+、K+、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为延长食品保质期,可向其中大量添加苯甲酸钠等防腐剂 | |
| B. | 催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生 | |
| C. | PM2.5是指空气中氮氧化物和硫氧化物含量之和 | |
| D. | “地沟油”可以制成肥皂,从而提高资源的利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4 能与水缓慢反应生成Fe(OH)3 和O2,故可用作水的消毒剂和净化剂 | |
| B. | 钢铁表面烤蓝生成一层致密的Fe3O4,能起到防腐蚀作用 | |
| C. | 太阳能、风能是可再生能源,应大力推广太阳能、风能的使用 | |
| D. | 新型能源生物柴油和矿物油的主要化学成分相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .若H 分子中所有碳原子均在一条直线上,则G 转化为H 的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O.
.若H 分子中所有碳原子均在一条直线上,则G 转化为H 的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液.实验操作过程如下:[废铁屑]$\stackrel{盐酸}{→}$[A溶液]$\stackrel{氯气}{→}$[氯气铁溶液]
某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液.实验操作过程如下:[废铁屑]$\stackrel{盐酸}{→}$[A溶液]$\stackrel{氯气}{→}$[氯气铁溶液]查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com