
【题目】某研究小组拟合成西他沙星的中间体X。其流程如下:
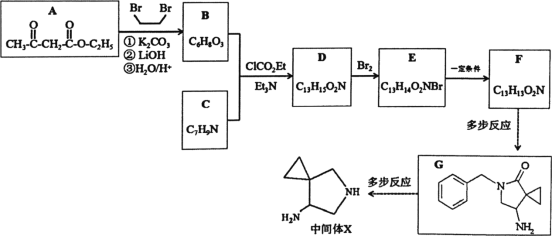
已知:①![]() +CH3CH2Br
+CH3CH2Br![]()

②R-CH2Br+![]()
![]()
![]() +HBr
+HBr
③![]() +H-CH2-COOR″
+H-CH2-COOR″![]() RCOCH2COOR″+R′-OH
RCOCH2COOR″+R′-OH
请回答:
(1)下列说法正确的是___。
A.化合物A不能与H2发生加成反应
B.化合物D→E,发生了取代反应
C.化合物F的水解产物具有两性
D.化合物G分子式为C13H15ON2
(2)化合物C的结构简式___。
(3)写出E→F的化学方程式___。
(4)中间体X有多种同分异构体,写出3种同时满足下列条件的X的同分异构体结构简式___。
①分子中含有一个六元碳环;②含有![]() 结构。
结构。
(5)以乙醇为原料,设计合成A的路线(无机试剂任选,用流程图表示)__。
【答案】BC ![]()
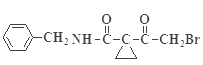
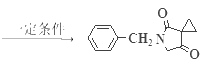 +HBr
+HBr ![]() 、
、![]() 、
、![]() 、
、![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]()
CH3COOCH2CH3![]() CH3COCH2COOCH2CH3
CH3COCH2COOCH2CH3
【解析】
根据![]() +CH3CH2Br
+CH3CH2Br![]()
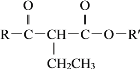 ,
,![]() 与1,2-二溴乙烷反应生成
与1,2-二溴乙烷反应生成![]() ,
,![]() 再水解为
再水解为![]() ,B是
,B是![]() ;由G的结构
;由G的结构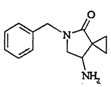 ,含有苯环,逆推C是
,含有苯环,逆推C是![]() ;
;![]() 与
与![]() 反应生成
反应生成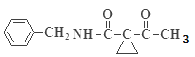 ,则D是
,则D是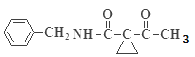 ,D与溴发生取代反应生成img src="http://thumb.1010pic.com/questionBank/Upload/2020/08/29/06/77129ef2/SYS202008290602056439762492_DA/SYS202008290602056439762492_DA.002.png" width="203" height="65" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" /> (E),根据R-CH2Br+
,D与溴发生取代反应生成img src="http://thumb.1010pic.com/questionBank/Upload/2020/08/29/06/77129ef2/SYS202008290602056439762492_DA/SYS202008290602056439762492_DA.002.png" width="203" height="65" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" /> (E),根据R-CH2Br+![]()
![]()
![]() +HBr ,E在一定条件下生成
+HBr ,E在一定条件下生成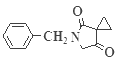 (F)。
(F)。
A.化合物A含有羰基,能与H2发生加成反应,故A错误;
B.化合物D→E,是D分子中1个氢原子被1个溴原子代替,发生了取代反应,故B正确;
C.化合物F是 ,含有肽键,水解产物含有氨基、羧基,所以具有两性,故C正确;
,含有肽键,水解产物含有氨基、羧基,所以具有两性,故C正确;
D.由G的结构简式 ,可知G分子式为C13H16ON2,故D错误。
,可知G分子式为C13H16ON2,故D错误。
选BC;
(2)由G的结构 ,含有苯环,逆推C是
,含有苯环,逆推C是![]() 。
。
(3)E是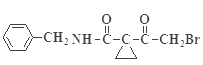 在一定条件下生成
在一定条件下生成 ,反应的化学方程式是
,反应的化学方程式是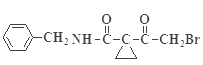
 +HBr。
+HBr。
(4)①分子中含有一个六元碳环;②含有![]() 结构的
结构的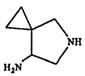 同分异构体有
同分异构体有![]() 、
、![]() 、
、![]() 、
、![]() ;
;
(5)乙醇氧化为乙醛、乙醛氧化为乙酸,乙醇和乙酸发生酯化反应生成乙酸乙酯,2分子乙酸乙酯在一定条件下反应生成![]() ,以乙醇为原料合成
,以乙醇为原料合成![]() 的路线图为CH3CH2OH
的路线图为CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3![]() CH3COCH2COOCH2CH3。
CH3COCH2COOCH2CH3。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】研究和深度开发CO、CO2的应用对建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)=2Fe(s)+3CO(g) ΔH1=+489.0kJmol-1,
C(s)+CO2(g)=2CO(g) △H2=+172.5kJmol-1
则CO还原Fe2O3(s)的热化学方程式为____________________。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:__________________。
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化见图1。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化见图1。
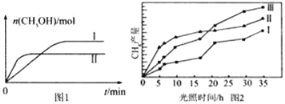
①线Ⅰ、Ⅱ对应的平衡常数大小关系为KI______KⅡ(填“>”或“=”或“<”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2、 c mol CH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为____________。
(4)利用光能和光催化剂,可将CO2和H2(g)转化为CH4和O2,紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化见图2。在0~15小时内,CH4的平均生成速率I、Ⅱ和Ⅲ从大到小的顺序为_____________(填序号)
(5)一种甲醇燃料电池,使用的电解质溶液是2mol·L-1的KOH溶液。
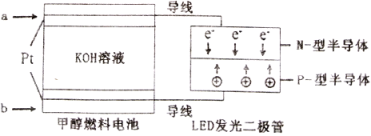
请写出加入(通入)b物质一极的电极反应式________________;每消耗6.4g甲醇转移的电子数为_______________。
(6)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的醋酸与bmol/LBa(OH)2溶液等体积混合后,溶液中:2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数Ka为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
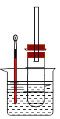
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1)用水浴加热而不直接用酒精灯加热的原因是_______________________________。
(2)观察到_________________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是_________________________________。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是______________________,检验的方法是_____________(需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 温度控制在500℃有利于合成氨反应
B. 用排饱和食盐水法收集Cl2
C. 打开碳酸饮料会有大量气泡冒出
D. 工业制取金属钾Na(l)+KCl(l) ![]() NaCl(l)+K(g)选取适宜的温度,使钾变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使钾变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)═2H2O(g)△H1
3H2(g)+Fe2O3(s)═2Fe(s)+3H2O(g)△H2
2Fe(s)+![]() O2(g)═Fe2O3(s)△H3
O2(g)═Fe2O3(s)△H3
2Al(s)+![]() O2(g)═Al2O3(s)△H4
O2(g)═Al2O3(s)△H4
2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0B.△H5<0,△H4<△H3
C.△H1=△H2+△H3D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将4.48L混合气体通入足量溴水,溴水质量增重2.8克,通过计算回答:
(1)据题意知混合气体的平均相对分子质量为___,则烷烃分子式为___;
(2)据题意知4.48L混合气体的质量为___克,烷烃的物质的量为___,烯烃的相对分子质量为___;
(3)混合气体中的烯烃分子式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土是一种重要的战略资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:
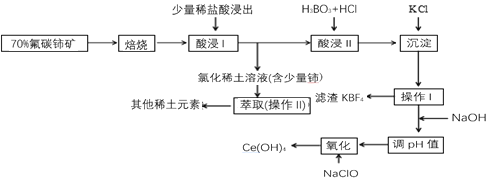
已知:
i.铈的常见化合价为+3、+4。焙烧后铈元素转化成CeO2和CeF4。四价铈不易进入溶液,而三价稀土元素易进入溶液。
ii.酸浸II中发生反应:9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是_______。
②焙烧后产生的CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2![]() CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:________。
CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:________。
(2)在酸浸I中用盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。少量铈进入稀土溶液发生反应的离子方程式是________。
(3)向Ce(BF4)3中加入KCl溶液的目的是______。
(4)操作I的名称为_______,在实验室中进行操作II时所需要的硅酸盐仪器有_______。
(5)“操作I”后,向溶液中加入NaOH溶液来调节溶液的pH,以获得Ce(OH)3沉淀,常温下加入NaOH调节溶液的pH应大于________即可认为Ce3+已完全沉淀。(已知:Ksp[Ce(OH)3]=1.0×10-20)
(6)取上述流程中得到的Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300mol FeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为______(已知氧化性:Ce4+>KMnO4;Ce(OH)4的相对分子质量为208,保留3位有效数字)。
(7)利用电解方法也可以实现铈的回收。在酸性条件下电解Ce2O3(如图),离子交换膜为____(填“阴”或“阳”)离子交换膜。
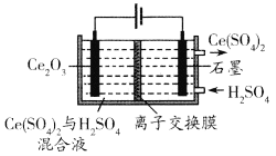
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 天然气、水煤气、液化石油气均是生活中常用的燃料,它们的主要成分都是化合物
B. “中国天眼”的“眼眶”是钢铁结成的圈梁,属于金属材料
C. 制玻璃和水泥都要用到石灰石原料
D. 1996年人工合成了第112号元素鎶(Cn),盛放鎶的容器上应该贴的标签是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
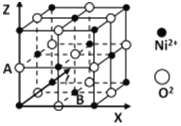
【题目】祖母绿是四大名贵宝石之一,主要成分为Be3Al2Si6O18,含有微量的Cr、Ni、Fe元素而呈现各种颜色。回答下列问题:
(1)基态Ni2+的电子排布式为_______________;宝石中Si的杂化方式是____。
(2)成键元素电负性差值越大,化学键离子性百分数越高,在卤素与Al组成的化合物中,离子性百分数最高的化合物是______(填化学式)。
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。Cr(CO)6的晶体类型是______,加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的作用力类型为_________。
(4)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用Δ表示),它与中心离子的结构、电荷、配体有关。试判断分裂能Δ[Fe(H2O)63+] _____ Δ[Fe(H2O)62+](填“>”“<”或“=”),理由是__________。
(5)氧化镍晶胞如图所示,A的原子坐标参数为:(0,0,![]() ),则底面面心B的原子坐标参数为______。
),则底面面心B的原子坐标参数为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com