
【题目】下图表示元素周期表的前三周期,表中的字母各代表一种元素,请回答下列问题:

①写出D单质的电子式____________;A与E的上一周期同主族元素形成的原子个数比为1:1的化合物的电子式_______________。
②E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________;
③A的最高价氧化物对应的水化物中所含化学键为___________________,其水溶液与B单质反应的离子方程式为___________________________;
④写出实验室制备F单质的化学方程式______________________________________。
⑤将Fe与C的一种单质(导体)用导线连接,共同浸入到食盐水中构成闭合回路,其中C极为_____极(填正或负),该电极反应式为:____________________。
⑥以D2H4和O2为原料,与KOH溶液形成的原燃料电池中,负极反应式为___________,
(生成物对环境友好无污染)
当外电路转移0.2 mol电子时,消耗的O2在标准状况下的体积为___________。
【答案】 ![]()
![]() HCl 离子键、共价键 2Al + 2OH - + 2H2O = 2AlO2- + 3H2↑ MnO2+4HCl(浓)
HCl 离子键、共价键 2Al + 2OH - + 2H2O = 2AlO2- + 3H2↑ MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O 正 O2+4e-+2H2O=4OH- N2H4 - 4e- + 4OH- = N2 +4H2O 1.12L
MnCl2+Cl2+2H2O 正 O2+4e-+2H2O=4OH- N2H4 - 4e- + 4OH- = N2 +4H2O 1.12L
【解析】由表可知,ABCDEF分别为钠、铝、碳、氮、硫、氯等元素。
①D单质氮气的电子式![]() ;A与E的上一周期同主族元素形成的原子个数比为1:1的化合物是过氧化钠,其电子式为
;A与E的上一周期同主族元素形成的原子个数比为1:1的化合物是过氧化钠,其电子式为![]() 。
。
②E和F分别形成的气态氢化物中较稳定的是HCl;
③A的最高价氧化物对应的水化物氢氧化钠中所含化学键为离子键、共价键,其水溶液与B单质反应的离子方程式为2Al + 2OH - + 2H2O = 2AlO2- + 3H2↑;
④实验室用浓盐酸和二氧化锰加热的方法制备氯气,化学方程式MnO2+4HCl(浓)![]() MnCl2+Cl2+2H2O 。
MnCl2+Cl2+2H2O 。
⑤将Fe与C的一种单质(导体)用导线连接,共同浸入到食盐水中构成闭合回路,类比钢铁的电化学腐蚀, C极为正极,该电极反应式为:O2+4e-+2H2O=4OH-。
⑥以D2H4和O2为原料,与KOH溶液形成的原燃料电池,因为生成物对环境友好无污染,可知产物为氮气和水,所以负极反应式为N2H4 - 4e- + 4OH- = N2 +4H2O ,当外电路转移0.2 mol电子时,消耗的O2在标准状况下的体积为1.12L 。


科目:高中化学 来源: 题型:
【题目】将2.56 g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12 L(标准状况),则反应过程中转移的电子为( )
A. 0.08 mol B. 0.16 mol C. 0.24 mol D. 0.32mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向某浓度的新制氯水中逐滴加入Na2SO3溶液,溶液pH 变化如图所示(整个过程中无气体逸出),下列关系正确的是( )

A. a点:c(H+)=c(Cl-)+c(OH-)
B. b点:c(Cl-)=0.005mol·L-1
C. c点:c(Na+)=2c(HSO3-)+2c(SO32-)+2c(SO42-)+2c(H2SO3)
D. d 点:c(Na+)>c(Cl-)>2c(SO32-)+c(HSO3-)+2c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)湿法制备高铁酸钠(Na2FeO4)的反应体系有六种微粒:Fe(OH)3、ClO-、OH-、FeO![]() 、
、
Cl-、H2O。
①写出并配平湿法制备高铁酸钠的离子方程式:__________________________。
②低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),最可能的原因是_________________________________________________________________。
(2)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是________________,氧化产物是____________,每生成1 mol Na2FeO4转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象的预测或装置的选用正确的是
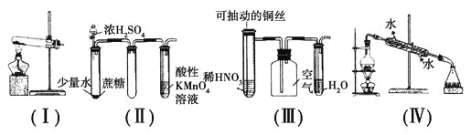
A.用装置(Ⅰ)加热草酸晶体获取某些气体(草酸晶体的熔点101.5 ℃,分解温度约为150 ℃)
B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产生空气污染
D.用装置(Ⅳ)分离溴苯和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法正确的是
A.元素周期表中有 8 个主族
B.IA 族中的元素全部是金属元素
C.第三周期有 8 种元素
D.短周期元素是指第一 、二周期所含有的全部元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将AlCl3溶液和NaOH溶液等体积混合,得到的沉淀物中所含铝元素的质量与溶液中所含铝元素的质量相等,则原AlCl3溶液和NaOH溶液物质的量浓度之比可能是
A. 1∶3 B. 2∶7 C. 1∶4 D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH4(g)+2O2(g)==CO2(g)+2H2O(l) △H=-Q1kJ·mol-1①
2H2(g)+O2(g)=2H2O(g) △H=-Q2kJ·mol-1②
2H2(g)+O2(g)=2H2O(l) △H=-Q3kJ·mol-1③
常温下,取体积比为4∶1的甲烷和氢气的混合气体11.2 L(标准状况),经完全燃烧后恢复到常温,放出的热量(单位:kJ)( )
A. 0.4Q1+0.05Q3 B. 0.4Q1+0.05Q2 C. 0.4Q1+0.lQ3 D. 0.4Q1+0.2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由Na、Mg、Al、Fe四种金属单质中的两种组成的混合物共12g,跟足量盐酸反应,产生5.6L H2(标准状况下),由此可判断混合物中必定含有( )
A. Na B. Mg C. Al D. Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com