
化学知识广泛应用于生产、生活中,下列叙述不正确的是
A.研发可降解高分子材料,减少“白色污染”
B.明矾和ClO2都能作为净水剂,其原理完全相同
C.海水淡化和工业生产及生活废水的再生利用,是解决缺水问题的有效途径
D.液氯罐泄漏时,可将其移入水塘中,并向水塘中加入生石灰
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年宁夏高二上学期期中化学试卷(解析版) 题型:选择题
下列晶体熔化时不需破坏化学键的是 ( )
A、晶体硅 B、食盐 C、固体碘 D、金属钾
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑
B、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓
C、铁片放入过量的稀硝酸中:3Fe+8H++2NO3-===3Fe2++2NO2↑+4H2O
D、FeCl2溶液跟Cl2反应:2Fe2++Cl2==2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末考试化学试卷(解析版) 题型:填空题
(1)用正确的序号填空: ①12C、13C、14C; ②红磷和白磷; ③H2O和D2O;④CH3CH2OH与CH3OCH3; ⑤CH4和CH3CH3 ;
互为同位素的是 ; 互为同素异形体的是 ;
互为同分异构体的是 ; 互为同系物的是
(2)由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不 断溶解 | C的质 量增加 | A上有气 体产生 |
根据实验现象回答下列问题:
①装置甲中作正极的是_____ ___ (填“A”或“B”) 。
②装置乙溶液中Cu2+向_____ __极移动(填“B”或“C”)。
③装置丙中金属A上电极反应属于___ ___(填“氧化反应”或“还原反应”)。
④四种金属活动性由强到弱的顺序是____ ___。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末考试化学试卷(解析版) 题型:选择题
如图是四种常见有机物分子的比例模型示意图。下列说法正确的是

A.甲是甲烷,甲烷的二氯取代产物只有一种结构
B.乙是乙烯,乙烯可与溴水发生取代反应使溴水褪色
C.丙是苯,苯结构比较稳定,不能发生氧化反应
D.丁是乙酸,一定条件下乙酸能跟乙醇发生酯化反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省宿迁市高二下学期期末考试化学试卷(解析版) 题型:选择题
下列物质中既含有离子键又含有共价键的化合物是
A.NaCl B.H2O C.KOH D.CH3Cl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高二下学期期末考试化学试卷(解析版) 题型:填空题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
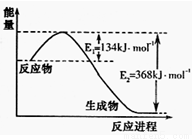
(1)下图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在一定体积的密闭容器中,进行如下化学反应: N2(g)+3H2(g) 2NH3(g)△H <0,
2NH3(g)△H <0,
其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | … |
K/(mol·L-1) | 4.1×106 | K1 | K2 | … |
完成下列问题:
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆)
B.2v(N2)(正)=v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O]+)> c(H+)>c(OH-)
C.2 c(N2H62+)+ c([N2H5·H2O]+)+ c(H+)= c(Cl-)+ c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省高二下学期期末考试化学试卷(解析版) 题型:选择题
某研究性学习小组欲用化学方法测量一个不规则容器的体积。把35.1 g NaCl放入 500 mL烧杯中,加入150 mL蒸馏水。待NaCl完全溶解后,将溶液全部转移到容器中,用蒸馏水稀释至完全充满容器。从中取出溶液100 mL,该溶液恰好与 20 mL 0.100 mol·L-1 AgNO3溶液完全反应。则该容器的体积为
A.30 L B.20 L C.10 L D.40 L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年中国石油天然气管道局中学高二下第二次月考化学试卷(解析版) 题型:选择题
下列对一些实验事实及其理论解释都正确的是:( )
选项 | 实验事实 | 理论解释 |
A | N原子的第一电离能小于O原子 | 同周期元素原子的电离能随原子序数增大而增大 |
B | HF的沸点低于HCl | HF的相对分子质量小于HCl |
C | 金刚石的熔点高于石墨 | 金刚石是原子晶体,石墨是分子晶体 |
D | CO2为直线形分子 | CO2分子中C为sp杂化,键角为180° |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com