
| A. | 石墨与O2生成CO2的反应是吸热反应 | |
| B. | 等量金刚石和石墨完全燃烧,金刚石放出热量更多 | |
| C. | 从能量角度看,金刚石比石墨更稳定 | |
| D. | 金刚石转化为石墨需要吸收的能量为E3-E2 |
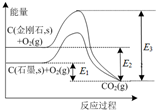
分析 根据图示可知,无论是金刚石的燃烧反应还是石墨的燃烧反应中,反应物的能量均高于生成物的能量,即均为放热反应;且金刚石的能量高于石墨的能量,根据物质的能量越高,则物质的稳定性越差,即可分析出金刚石和石墨的稳定性问题,据此分析.
解答 解:A、石墨与O2的总能量高于CO2的能量,故石墨与O2生成CO2反应为放热反应,故A错误;
B、根据图示可知,金刚石的能量高于石墨的能量,故等量的金刚石和石墨燃烧时,金刚石放出的热量更多,故B正确;
C、物质的能量越高则物质越不稳定,故金刚石的稳定性比石墨差,故C错误;
D、根据图示可知,金刚石的能量高于石墨的能量,故金刚石转化为石墨是放出能量,故D错误.
故选B.
点评 本题考查了根据图象来分析反应的吸放热并根据物质的能量来分析物质的稳定性,难度不大,注意基础的掌握.


科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子结构中不存在手性碳 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子中的氢原子均可被钠置换 | |
| B. | 乙醇能与钠反应放出氢气,说明乙醉能电离出H+而表现酸性 | |
| C. | 乙醇分子羟基中的氢原子比乙烷分子中的氢原子活泼 | |
| D. | 乙醇分子羟基中的氢原子比水分子中的氢原子活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
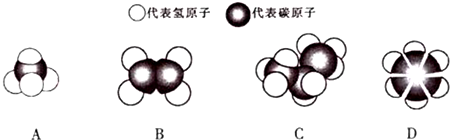
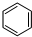 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$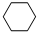 .
. .
.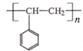 路线流程图(无机试剂任选).合成路线流程图示例如下:
路线流程图(无机试剂任选).合成路线流程图示例如下: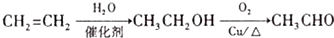
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
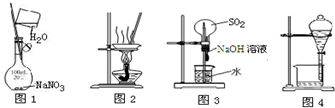
| A. | 用图1所示装置配制一定物质的量浓度的NaNO3溶液 | |
| B. | 用图2所示装置蒸发MgCl2溶液制备无水MgCl2 | |
| C. | 用图3所示装置可以完成“喷泉”实验 | |
| D. | 苯萃取碘水中的碘后,从图4装置下口放出的是碘的苯溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
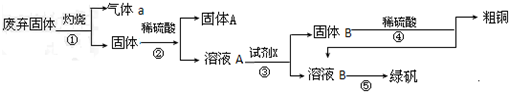
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
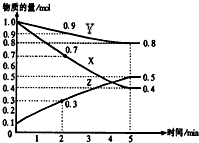 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com