
| A.电解精炼铜时是将电能转化为化学能,电路中每通过2mole-时,阳极就会溶解64克铜 |
| B.电解精炼铜时阳极为精铜,阴极为粗铜,电解过程中电解质不需要更换 |
| C.在铁质器皿上镀铝,电解质为熔融氧化铝,铁制器皿作阴极,阳极为铝棒 |
| D.电镀过程中电镀液需要不断更换 |
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4(Cu(OH)2) | B.NaOH(NaOH) | C.NaCl(H2O) | D.CuCl2(CuCl2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.28L | B.0.56L | C.0.14L | D.11.2L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
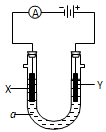
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
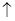 。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
| B.玻璃钢、航天飞机上的隔热陶瓷瓦都属于复合材料 |
| C.氧化钠可作为呼吸面具和潜水艇里氧气的来源 |
| D.铝—空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
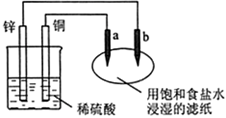
| A.a是正极,发生还原反应,b是阴极,发生还原反应 |
| B.装置工作时,稀硫酸溶液中C(H+)变小、C(Cu2+)变大 |
| C.往滤纸上滴加酚酞试液,a极附近颜色变红 |
| D.稀硫酸中硫酸根离子的物质的量不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀NaOH溶液 | B.HCl溶液 | C.CuSO4溶液 | D.酸性AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
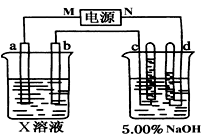
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com