
����Ŀ��������ij���ʵ�ת����Ϊ���ĵ��ĸ����ʵ���ռ��ʼʱ�����ʵ�ԭ���ʵ����İٷֱȣ���֪�ϳɰ���ӦΪN2��g��+3H2��g��2NH3��g������һ���Ϊ10L���ݻ�������ܱ������з���1mol N2��3mol H2 �� ��һ�������·�����Ӧ����4min�ﵽ��ѧƽ��״̬����������а��������ʵ���Ϊ0.6mol����
��1��������ת���ʣ�
��2����������ʾƽ����Ӧ�����Ƕ��٣�
��3��ƽ��״̬ʱ���������ʵ���Ũ�ȣ�
���𰸡�
��1���⣺��4min�ﵽ��ѧƽ��״̬����������а��������ʵ���Ϊ0.6mol����
N2��g��+ | 3H2��g�� | 2NH3��g�� | ||
��ʼ | 1 | 3 | 0 | |
ת�� | 0.3 | 0.9 | 0.6 | |
ƽ�� | 0.7 | 2.1 | 0.6 |
������ת����Ϊ ![]() ��100%=30%��
��100%=30%��
�ʴ�Ϊ��������ת����Ϊ30%��
��2���⣺��������ʾƽ����Ӧ������ ![]() =0.0225 mol��Lmin����1��
=0.0225 mol��Lmin����1��
����������ʾƽ����Ӧ������0.0225 mol��Lmin����1��
��3���⣺ƽ��״̬ʱ���������ʵ���Ũ��Ϊ ![]() =0.21 mol/L��
=0.21 mol/L��
��ƽ��״̬ʱ���������ʵ���Ũ��Ϊ0.21mol/L��
����������4min�ﵽ��ѧƽ��״̬����������а��������ʵ���Ϊ0.6mol����
N2��g��+ | 3H2��g�� | 2NH3��g�� | ||
��ʼ | 1 | 3 | 0 | |
ת�� | 0.3 | 0.9 | 0.6 | |
ƽ�� | 0.7 | 2.1 | 0.6 |
����1��ת����= ![]() ��100%����2�����v=
��100%����2�����v= ![]() ���㣻��3�����c=
���㣻��3�����c= ![]() ���㣮
���㣮
�����㾫�������ջ�ѧƽ��ļ����ǽ����ĸ�������Ҫ֪����Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е����λ����ͼ������˵����ȷ���ǣ� �� 
A.Y��Z�ij����������ͨ�����������NaOH��Һ������
B.���⻯����ȶ���������ǿ��˳����Q��W��Z
C.Ԫ��Y��Z��W��Q��ԭ�Ӱ뾶��������
D.Y��������������ʢװW������������Ӧ��ˮ�����Ũ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���һ�������¼��ܷ���������Ӧ�����ܷ���ˮ���������Ӧ���ǣ� ��
A.��������
B.������
C.�������
D.����ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼʾ��ת����ϵ����֪CΪ�ܶ���С�����壬���ǵ���ʡ�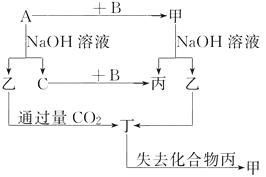
����ͼʾת����ϵ�ش�
��1��д���������ʵĻ�ѧʽ��
A �� B �� �� �� ����
��2����ɵ���A��Ԫ�������ڱ��е�λ���� �� ���ĵ���ʽ����
��3��д�����б仯�ķ���ʽ��
��A��NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��
���������CO2��Ӧ�����ӷ���ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ����Ҫ�ɷ�ΪMg2B2O5��H2O��������A12O3��Fe3O4����ȡ����Ĺ�������Ϊ��
��֪�������������������ƣ�Ҳ��������������Һ��Ӧ��![]()
��BCl3���۵�Ϊ-107��3�棬�е�Ϊl2��5�棬�ڳ�ʪ���������γɰ�����
I���ش��������⣺
��1��֤����ҺB�к�����Ԫ�صķ�����
��2��Mg��X��Ӧ��ȡ����Ļ�ѧ����ʽ
��3����ͼ����ȡMgCl2�ġ�һ����������ָ
��4��II��ijͬѧ�����ͼ��ʾװ���Ʊ����Ȼ���
�ش��������⣺
Eװ�õ�������
��5�����ȥ��Bװ�ã����ܵĺ������
��6��Eװ�ú��滹Ӧ���ӵ�һ��װ������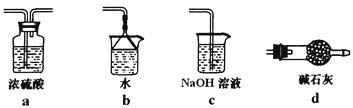
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����������������ԴΣ������Щ���п�ʼ�������Ҵ�(C2H5OH)��������������ȼ�ϡ��Ҵ��Ĺ�������( )
A. ��CH3 B. ��COOH C. ��OH D. H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���� ( )
A.ʯ���ѽ⡢ʯ�ͷ���ú�ĸ����ǻ�ѧ�仯
B.��װ�ò��Ͼ���ϩ�;�����ϩ��������
C.��һ�������£�����Һ�塢�������������屽��������������ȡ����Ӧ
D.���ͼױ��������ڷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����(Rb)��������ȷ����
A. ��λ�����ڱ��ĵ������ڡ��ڢ�A��B. ���ơ��ء��3�ֵ����У�卑��۵����
C. �������������D. ����������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚϣ�����ȷ���ǣ� ��
A.���ȶ��ԣ�HBr��HCl
B.���ԣ�Al��OH��3��Mg��OH��2
C.�����ԣ�O��F
D.��ԭ�ԣ�S2����O2��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com