
| O | F |
| S | Cl |
| Se | Br |
| Te | I |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:不详 题型:实验题
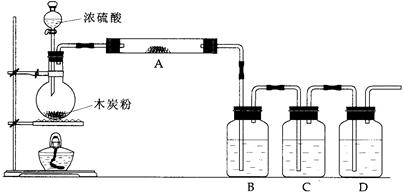
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2漂白了滤纸 | B.化学反应放热蒸发了溴 |
| C.SO2与溴化合生成无色物质 | D.SO2与溴发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 KOH+I2+O2(未配平),下列说法正确的是( )
KOH+I2+O2(未配平),下列说法正确的是( )| A.O3在反应中被氧化成O2 |
B.1 mol O3在反应中只有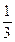 mol的氧原子化合价发生了变化 mol的氧原子化合价发生了变化 |
| C.1 mol O3在反应中得到2 mol电子 |
| D.反应中氧化产物与还原产物的物质的量之比为2∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
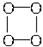 ),有关O4的说法正确的是( )
),有关O4的说法正确的是( )| A.O4的摩尔质量64 g | B.O4与O2互为同位素 |
| C.相同质量的O4与O3所含原子个数比为4∶3 | D.O4与O3、O2都是氧元素的同素异形体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
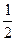 O2(g)
O2(g) SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)
SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 矿渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com