

分析 (1)根据亚铁离子具有强还原性和在水溶液中易发生水解作答;
(2)①根据配制一定物质的量浓度溶液实验用到的仪器回答;
②滴定实验中,待测液放在锥形瓶中,高锰酸钾溶液具有强氧化性,放在酸式滴定管中,不用加指示剂,利用高锰酸钾溶液本身的颜色即可;
(3)①H2O2与亚铁离子反应生成铁离子和水,以此写出离子方程式即可;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量;
③先求出氧化铁中铁的质量,根据铁原子守恒可知硫酸亚铁的质量,然后求硫酸亚铁的质量分数即可.
解答 解:(1)亚铁离子具有强还原性,容易被空气中的氧气氧化,糖衣可以隔绝空气,防止亚铁离子被氧气氧化,亚铁离子在水溶液中易水解,加盐酸增大氢离子浓度可以抑制水解,
故答案为:隔绝空气,防止被O2氧化;防止Fe2+水解;
(2)①配制一定物质的量浓度溶液实验用到的仪器除托盘天平、烧杯、玻璃棒、量筒外,还需要250mol容量瓶和定容时使用的胶头滴管,
故答案为:250ml容量瓶;胶头滴管;
②滴定实验中,待测液放在锥形瓶中,因此含硫酸亚铁的滤液放在锥形瓶,高锰酸钾溶液具有强氧化性,放在酸式滴定管中;不用加指示剂,利用高锰酸钾溶液本身的颜色即可,当加入最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点,
故答案为:锥形瓶;酸式滴定管;不用加;最后一滴酸性高锰酸钾溶液时,锥形瓶中溶液的颜色变为紫色,震荡,且半分钟内不恢复原色,则滴定到了终点;
(3)①H2O2与亚铁离子反应生成铁离子和水,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②从红褐色的悬浊液过滤得到含氢氧化铁的滤渣,洗涤除掉吸附的杂质离子,灼烧分解生成氧化铁,冷却后称量,
故答案为:A、B、F、E;
③氧化铁中铁元素的质量为:0.8960g×$\frac{112}{160}$=0.6272g,根据铁元素守恒可知硫酸亚铁中铁元素的质量为0.6272g,则硫酸亚铁的质量为:0.6272g×$\frac{152}{56}$=1.7024g,因此硫酸亚铁的质量为:$\frac{1.7024g}{0.3g×10}$×100%=56.7%,
故答案为:56.7%.
点评 本题考查亚铁离子的性质,涉及亚铁离子的强还原性、水解反应和实验仪器的选取、实验步骤的设计和滴定终点的确定,计算硫酸亚铁质量分数根据铁元素守恒计算可减少计算工作量.


科目:高中化学 来源: 题型:选择题
| A. | 平衡后CO的体积分数为40% | |
| B. | 平衡后CO的转化率为25% | |
| C. | 平衡后水的转化率为50% | |
| D. | 平衡后混合气体的平均相对分子质量为24 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 它的一氯代物只有一种同分异构体 | |
| B. | 它的二氯代物有两种同分异构体 | |
| C. | 它的分子式为C8H8 | |
| D. | 它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,平衡时若充入稀有气体,SO2的转化率增大 | |
| B. | 0~6 min的平衡反应速率:v(O2)=0.105 mol/(L•min) | |
| C. | 保持其他条件不变,仅降低温度,正反应速率减小程度比逆反应速率减小程度大 | |
| D. | 反应开始时,向容器中通入的SO2的物质的量是1.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
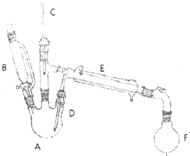 溴乙烷是有机合成的重要原料,实验室合成溴乙烷的装置示意图、相关原理和数据如下:
溴乙烷是有机合成的重要原料,实验室合成溴乙烷的装置示意图、相关原理和数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解度 | |
| 乙醇 | 46 | 0.789 | 78.3 | 易溶 |
| 溴乙烷 | 109 | 1.46 | 38.2 | 难溶 |
| 浓硫酸(H2SO4) | 98 | 1.84 | 338.0 | 易溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O4(g)═2NO2(g),改变某一条件后,气体颜色加深 | |
| B. | H2(g)+I2(g)═2HI(g),单位时间内消耗H2和HI的物质的量之比大于1:2 | |
| C. | N2(g)+3H2(g)═2NH3(g),改变某一条件后,NH3的体积分数增加 | |
| D. | 2SO2(g)+O2(g)═2SO3(g),恒温恒压条件下,充入He |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com