
 氮元素是一种常见元素,能形成多种化合物.
氮元素是一种常见元素,能形成多种化合物.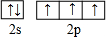 ,等物质的量的NH3和N2组成的混合气体中σ键和π键的物质之比为2:1.
,等物质的量的NH3和N2组成的混合气体中σ键和π键的物质之比为2:1.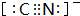 .
.分析 (1)基态氮原子最外层电子排布式为2s22p3,根据泡利原理与洪特规则画出最外层电子排布图;
NH3分子含有含有3个σ键,N2分子中含有1个σ键、2个π键;
(2)CN-与N2互为等电子体,CN-中原子与N原子之间形成3对共用电子对;
(3)同种元素含氧酸,中心元素化合价越高,对N-O-H中O原子的单子吸引更强;
(4)①同周期随原子序数增大,元素第一电离能呈增大趋势,当ⅡA族的s能级为全满稳定状态,ⅤA族的p能级为半满稳定状态,第一电离能高于同周期相邻元素的;
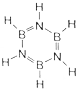
②环硼氮六烷中BN原子形成3个σ键、N原子形成3个σ键,均没有孤对电子;
(5)立方氮化硼晶体结构与金刚石相似,硬度与金刚石相当,立方氮化硼属于原子晶体;金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原子,立方体内部还有4个碳原子,如图所示: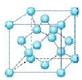 ,所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8}$+6×$\frac{1}{2}$+4=8,立方氮化硼中氮原子与周围的4个硼原子形成四面体结构、硼原子与周围的4个氮原子形成四面体结构,因此立方氮化硼晶胞中应该含有4个N和4个B原子,计算BN晶胞的质量、晶胞的体积,根据ρ=$\frac{m}{ρ}$计算密度.
,所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8}$+6×$\frac{1}{2}$+4=8,立方氮化硼中氮原子与周围的4个硼原子形成四面体结构、硼原子与周围的4个氮原子形成四面体结构,因此立方氮化硼晶胞中应该含有4个N和4个B原子,计算BN晶胞的质量、晶胞的体积,根据ρ=$\frac{m}{ρ}$计算密度.
解答 解:(1)基态氮原子最外层电子排布式为2s22p3,根据泡利原理与洪特规则,最外层电子排布图我 ;NH3分子含有含有3个σ键,N2分子中含有1个σ键、2个π键,则等物质的量的NH3和N2组成的混合气体中σ键和π键的物质之比为(3+1)mol:2mol=2:1,
;NH3分子含有含有3个σ键,N2分子中含有1个σ键、2个π键,则等物质的量的NH3和N2组成的混合气体中σ键和π键的物质之比为(3+1)mol:2mol=2:1,
故答案为: ;2:1;
;2:1;
(2)CN-与N2互为等电子体,CN-中原子与N原子之间形成3对共用电子对,CN-的电子式: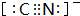 ,
,
故答案为: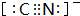 ;
;
(3)HNO3比HNO2中N元素为+3价,HNO3中N原子为+5价,HNO3中N元素正电荷更高,导致N-O-H中O原子的单子偏向N原子,更易电离出H+,HNO3比HNO2的酸性强,
故答案为:HNO2中N元素为+3价,HNO3中N原子为+5价,HNO3中N元素正电荷更高,导致N-O-H中O原子的单子偏向N原子,更易电离出H+;
(4)①同周期随原子序数增大,元素第一电离能呈增大趋势,当ⅡA族的s能级为全满稳定状态,ⅤA族的p能级为半满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能介于B、N之间的第二周期元素有Be、C、O三种元素,第一电离能为O>C>Be,
故答案为:O>C>Be;
②无机苯分子中B原子的价层电子对数是3且不含孤电子对,所以B原子属于sp2杂化,N原子的价层电子对数也是3且不含孤电子对,所以N原子属于sp2杂化,
故答案为:sp2;sp2;
(5)立方氮化硼晶体结构与金刚石相似,硬度与金刚石相当,立方氮化硼属于原子晶体;金刚石晶胞是立方体,其中8个顶点有8个碳原子,6个面各有6个碳原子,立方体内部还有4个碳原子,如图所示: ,所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8}$+6×$\frac{1}{2}$+4=8,立方氮化硼中氮原子与周围的4个硼原子形成四面体结构、硼原子与周围的4个氮原子形成四面体结构,因此立方氮化硼晶胞中应该含有4个N和4个B原子,B原子最外层有3个电子,形成4个共价键,含有1个配位键,则B原子与N原子之间共价键与配位键的数目比为3:1,BN晶胞中的质量为4×$\frac{25}{{N}_{A}}$,一个立方氮化硼晶胞的体积是(3.615×10-10cm)3,因此立方氮化硼的密度=4×$\frac{25}{{N}_{A}}$÷(3.615×10-10cm)3=$\frac{25×4}{(3.615×1{0}^{-10})^{3}×{N}_{A}}$g•cm-3,
,所以金刚石的一个晶胞中含有的碳原子数=8×$\frac{1}{8}$+6×$\frac{1}{2}$+4=8,立方氮化硼中氮原子与周围的4个硼原子形成四面体结构、硼原子与周围的4个氮原子形成四面体结构,因此立方氮化硼晶胞中应该含有4个N和4个B原子,B原子最外层有3个电子,形成4个共价键,含有1个配位键,则B原子与N原子之间共价键与配位键的数目比为3:1,BN晶胞中的质量为4×$\frac{25}{{N}_{A}}$,一个立方氮化硼晶胞的体积是(3.615×10-10cm)3,因此立方氮化硼的密度=4×$\frac{25}{{N}_{A}}$÷(3.615×10-10cm)3=$\frac{25×4}{(3.615×1{0}^{-10})^{3}×{N}_{A}}$g•cm-3,
故答案为:4;4;3;3:1;$\frac{25×4}{(3.615×1{0}^{-10})^{3}×{N}_{A}}$.
点评 本题是对物质结构的考查,涉及核外电子排布、电离能、分子空间构型、杂化类型的判断、晶胞结构以及晶胞的有关计算,(4)为易错点,注意熟记中学常见晶胞结构,注意同周期第一电离能异常情况,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Cu2+、SO42-、OH-、K+ | B. | Fe3+、SCN-、Cl-、H+ | ||
| C. | K+、CO32-、Cl-、H+ | D. | H+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾投入水中的电离方程式为:KAI(SO4)2•12H2O=K++Al3++2SO42-+12H20,说明明矾是一种混合物 | |
| B. | 净水时Al3+发生水解生成的是Al(OH)3沉淀 | |
| C. | 明矾净水的原理是杀菌消毒 | |
| D. | 硫酸铁可以代替明矾进行净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
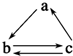 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| 物质 选项 | a | b | c |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | H2SO4 | SO2 | SO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
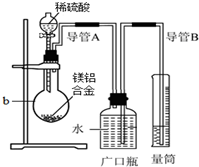 化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.
化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 mol/(L•s) | B. | 0.08 mol/(L•s) | C. | 0.16 mol/(L•s) | D. | 0.8 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 坐标对应点 | a | b | c | d |
| n(SO32-):n(HSO32-) | / | 91:9 | 1:1 | 9:91 |
| pH | >8.2 | 8.2 | 7.2 | 6.2 |
| A. | b点溶液中:水电离出的c(OH-)=1×10-5.8mol/L | |
| B. | c点溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) | |
| C. | d点溶液中HSO3-的电离大于水解 | |
| D. | d点溶液中:c(Na+)<c(SO32-)+c(HSO3-)+c(Cl-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com