


科目:高中化学 来源: 题型:
| A、C (K+)+C(H+)=C(S2-)+C(HS-)+C(OH-) |
| B、C(K+)+C (S2-)=0.3mol/L |
| C、C(K+)=C(S2-)+C (HS-)+C (H2S) |
| D、C(OH-)=C(H+)+C(HS-)+2C(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
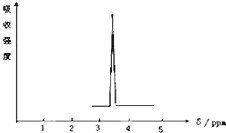 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量钠应保存在煤油中,实验后剩余的钠需放回原瓶 |
| B、2.3g钠与97.7g 水反应后溶液中溶质的质量分数等于4% |
| C、钠与CuSO4溶液反应生成的蓝色沉淀上有时出现暗斑,这是析出的金属铜 |
| D、用一般的化学还原法不能制取金属钠,但可用电解饱和NaCl溶液的方法制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2是氧化物,不是碱性氧化物 |
| B、Na2CO3不是碱,是一种钠盐 |
| C、NaOH是一元碱、强碱 |
| D、NaClO是氧化性盐、含氧酸盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com