
ČēĶ¼×°ÖĆ£¬A”¢BÖŠµē¼«ĪŖ¶ąæ׵ĶčŠŌµē¼«£»C”¢DĪŖ¼ŠŌŚŹŖµÄNa2SO4ĀĖÖ½ĢõÉĻµÄ²¬¼Š£»µēŌ“ÓŠa”¢bĮ½¼«”£ČōŌŚA”¢BÖŠ³äĀśKOHČÜŅŗŗóµ¹Į¢ÓŚKOHČÜŅŗµÄĖ®²ŪÖŠ£¬ĒŠ¶ĻK1£¬±ÕŗĻK2”¢K3£¬ĶØÖ±Į÷µē£¬Ņ»¶ĪŹ±¼äŗóŹŌ¹ÜÖŠ²śÉśĘųĢ壬ČēĶ¼ĖłŹ¾£¬¾Ż“Ė·ÖĪö£ŗ
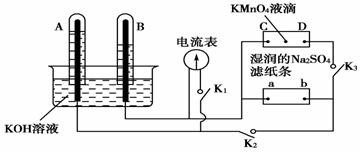
(1) BŹŌ¹ÜÖŠµÄĘųĢåŹĒ_______£ØĢīĆū³Ę»ņ·Ö×ÓŹ½£©£»aĪŖµēŌ“________(Õż»ņøŗ)¼«”£
(2)Š“³öµē½āŹ±A¼«µÄµē¼«·“Ó¦Ź½£ŗ _________________________________________”£
(3)Čōµē½āŅ»¶ĪŹ±¼ä£¬A”¢BÖŠ¾łÓŠĘųĢå°üĪ§µē¼«”£“ĖŹ±ĒŠ¶ĻK2”¢K3£¬±ÕŗĻK1”£µēĮ÷±ķµÄÖøÕėĘ«×Ŗ£¬Ōņ“ĖŹ±B¼«µē¼«·“Ó¦Ź½ĪŖ____________________________________________”£
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ij»ÆѧŠĖȤŠ”×éŌŚŹµŃéŹŅĢõ¼žĻĀŅŌĮņĖįĶČÜŅŗĪŖµē½āŅŗ£¬ÓƵē½āµÄ·½·ØŹµĻÖĮĖ“ÖĶ(ŗ¬ÓŠÉŁĮæµÄŠæ”¢Ģś”¢Ņų”¢½šµČ½šŹōŗĶÉŁĮææóĪļŌÓÖŹ)µÄĢį“棬²¢¶ŌŃō¼«ÄąŗĶµē½āŅŗÖŠ½šŹō½ųŠŠ»ŲŹÕŗĶŗ¬Įæ²ā¶Ø”£Ēė»Ų“šŅŌĻĀĪŹĢā”£
£Ø1£©µē½āŹ±£¬“ÖĶÓ¦ÓėµēŌ“µÄ ¼«ĻąĮ¬£¬Ņõ¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ £»µē½ā¹ż³ĢÖŠ£¬ĮņĖįĶµÄÅØ¶Č»į (Ń”Ģī”°±ä“ó”±”°²»±ä”±»ņ”°±äŠ””±)”£
£Ø2£©µē½āĶź³Éŗó£¬øĆŠ”×éĶ¬Ń§½«µē½āŅŗ¹żĀĖŗó¶ŌĀĖŅŗŗĶŃō¼«Äą·Ö±š½ųŠŠ“¦Ąķ£ŗ
¢ŁŃō¼«ÄąµÄ×ŪŗĻĄūÓĆ£ŗĻ”ĻõĖį“¦ĄķŃō¼«ÄąµĆµ½ĻõĖįŅųĻ”ČÜŅŗ£¬ĒėÄ抓³öøĆ²½·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
¢ŚCuµÄ»ŲŹÕ”¢ĀĖŅŗ³É·Ö¼°ŗ¬ĮæµÄ²ā¶Ø£ŗŅŌĻĀŹĒøĆŠ”×éÉč¼ĘµÄŅ»øöŹµŃéĮ÷³Ģ”£
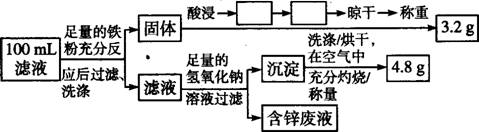
ŌŚÉĻŹöĮ÷³ĢÖŠæÕøńÄŚĢīÉĻĻąÓ¦µÄ²Ł×÷£ŗ ”¢ £»100 mLĀĖŅŗÖŠCu2+µÄÅضČĪŖ mol/l£¬Fe2+µÄÅضČĪŖ mol/l”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«“ÅŠŌŃõ»ÆĢś·ÅČėĻ”HNO3ÖŠæÉ·¢ÉśČēĻĀ·“Ó¦£ŗ 3Fe3O4+28HNO3 = 9Fe£ØNO3£©x+NO”ü +14H2O£¬ĻĀĮŠÅŠ¶ĻŗĻĄķµÄŹĒ
A£®Fe£ØNO3£©xÖŠµÄxĪŖ2
B£®Ļ”HNO3ŌŚ·“Ó¦ÖŠÖ»±ķĻÖŃõ»ÆŠŌ
C£®“ÅŠŌŃõ»ÆĢśÖŠµÄĖłÓŠĢśŌŖĖŲČ«²æ±»Ńõ»Æ
D£®·“Ó¦ÖŠĆ滹Ō0£®3molŃõ»Æ¼Į£¬¾ĶÓŠ0£®9molµē×Ó×ŖŅĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŅĶ¼ŹĒŅ»æī±Ź¼Ē±¾µēÄŌĖłÓĆ¼×“¼Č¼ĮĻµē³ŲµÄ½į¹¹Ź¾ŅāĶ¼”£
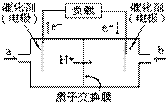
¼×“¼ŌŚ“߻ƼĮ×÷ÓĆĻĀĢį¹©ÖŹ×Ó(H+)ŗĶµē×Ó£¬µē×Ó¾ĶāµēĀ·”¢ÖŹ×Ó¾ÄŚµēĀ·µ½“ļĮķŅ»¼«ÓėŃõĘų·“Ó¦£¬µē³Ų×Ü·“Ó¦ĪŖ£ŗ
2CH3OH£«3O2 = 2CO2£«4H2O ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ÓŅµē¼«ĪŖµē³ŲµÄÕż¼«£¬b“¦ĶØČėµÄĪļÖŹŹĒæÕĘų
B£®×óµē¼«ĪŖµē³ŲµÄøŗ¼«£¬a“¦ĶØČėµÄĪļÖŹŹĒæÕĘų
C£®Õż¼«·“Ó¦Ź½ĪŖ£ŗCH3OH£«H2O£6e£ = CO2£«6H£«
D£®Õż¼«·“Ó¦Ź½ĪŖ£ŗO2+2H2O+4e£=4OH£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŹŅĪĀĻĀ£¬¶ŌÓŚ0.10 mol·L-1µÄ°±Ė®£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
A£®ÓėAlCl3ČÜŅŗ·“Ó¦·¢ÉśµÄĄė×Ó·½³ĢŹ½ĪŖ Al3++3OH—=Al(OH)3”ż
B£®¼ÓĖ®Ļ”ŹĶŗó£¬ČÜŅŗÖŠc(NH4+)·c(OH-) ±ä“ó
C£®ÓĆHNO3ČÜŅŗĶźČ«ÖŠŗĶŗó£¬ČÜŅŗ²»ĻŌÖŠŠŌ
D£®ĘäČÜŅŗµÄPH=13
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®ĮņĖįŗĶĮ×ĖįµÄĦ¶ūÖŹĮæ²»ĻąµČ
B£®18 gĖ®ÖŠŗ¬ÓŠ1 molĖ®
C£®O2µÄĦ¶ūÖŹĮæ(µ„Ī»ŹĒg”¤mol£1)ŌŚŹżÖµÉĻµČÓŚĘäĻą¶Ō·Ö×ÓÖŹĮæ
D£®1 mol COµÄÖŹĮæŹĒ28 g”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·“Ó¦ÖŠ£¬²»ÄܲśÉśĒāĘųµÄŹĒ£Ø £©
A. ŗģČȵÄĢśÓėĖ®ÕōĘų B. ÄĘÓėĖ®
C. ĀĮŗĶNaOHČÜŅŗ·“Ó¦ D. ĢśÓėĻ”ĻõĖį·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
·“Ó¦3CO + Fe2O3 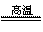 2Fe + 3CO2æÉÓĆÓŚ¹¤ŅµÉĻĮ¶Ģś£¬øĆ·“Ó¦ŹōÓŚ
2Fe + 3CO2æÉÓĆÓŚ¹¤ŅµÉĻĮ¶Ģś£¬øĆ·“Ó¦ŹōÓŚ
A£®ÖĆ»»·“Ó¦ B£®ø“·Ö½ā·“Ó¦ C£® »ÆŗĻ·“Ó¦ D£®Ńõ»Æ»¹Ō·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĶʶĻÕżČ·µÄŹĒ
A£®ÓÉH+(aq)+OH-(aq)=H20£Ø1£© ”÷H=-57£®3 kJ”¤mol-1£¬æÉÖŖŗ¬1 mo1 CH3COOHµÄČÜŅŗÓėŗ¬1 mol NaOHµÄČÜŅŗ»ģŗĻ£¬·Å³öČČĮæĪŖ57£®3 kJ
B£®ÓÉC(ŹÆÄ«)=C(½šøÕŹÆ) ”÷H=+1£®9 kJ”¤mol-1£¬æÉÖŖŹÆÄ«±Č½šøÕŹÆøüĪȶØ
C£®ÓÉN2(g)+3H2(g)=2NH3(g) ”÷H=-92£®4 kJ”¤mol-1£¬æÉÖŖ½«1 mol N2(g)ŗĶ3 mol H2(g)ÖĆÓŚĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó·Å³öČČĮæĪŖ92£®4 kJ
D£®ÓÉ”÷G£½”÷H-T”÷SæÉÖŖ£¬ĖłÓŠµÄ·ÅČČ·“Ó¦¶¼ÄÜ×Ō·¢½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com