
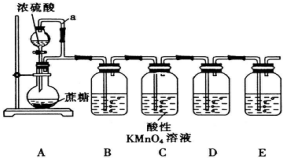
分析 装置A浓硫酸滴入蔗糖碳化放热,生成的碳和浓硫酸反应生成二氧化碳、二氧化硫和水,通过装置B中的品红检验二氧化硫的存在,通过装置C中高锰酸钾溶液除去二氧化硫,装置D中品红溶液检验二氧化硫是否除净,装置E中澄清石灰水变浑浊证明生成二氧化碳,
(1)装置 A 中盛放浓硫酸的仪器是添加浓硫酸的分液漏斗,a导气管是平衡压强使浓硫酸顺利流下;
(2)浓硫酸与水作用放出热量,升高了温度,加快了化学反应速率;浓硫酸具有脱水性,将蔗糖脱水后生成碳,碳与浓硫酸反应生成二氧化碳、二氧化碳和水,据此写出反应的化学方程式;
(3)检验反应的气体产物,通过装置B中的品红检验二氧化硫的存在,通过装置C中高锰酸钾溶液除去二氧化硫,装置D中品红溶液检验二氧化硫是否除净,装置E中澄清石灰水变浑浊证明生成二氧化碳,
解答 解:(1)装置 A 中盛放浓硫酸的仪器是添加浓硫酸的分液漏斗,a导气管是平衡压强使浓硫酸顺利流下;
故答案为:分液漏斗;平衡压强使浓硫酸顺利流下;
(2)向盛有蔗糖的烧杯中加几滴水后,水与浓硫酸作用,使温度升高,加快化学反应速率,浓硫酸具有脱水性和强氧化性,先将蔗糖脱水生成碳,反应为:C12H22O11$\stackrel{浓硫酸}{→}$12C+11H20,然后浓硫酸与碳反应生成二氧化碳、二氧化硫、水,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+SO2↑+2H20,
故答案为:水与浓硫酸作用,使温度升高,加快化学反应速率;C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+SO2↑+2H20;
(3)检验反应的气体产物,通过装置B中的品红检验二氧化硫的存在,通过装置C中高锰酸钾溶液除去二氧化硫,装置D中品红溶液检验二氧化硫是否除净,装置E中澄清石灰水变浑浊证明生成二氧化碳,装置 B、E 中所盛的试剂分别是品红溶液,澄清石灰水,装置 C 中发生反应的离子方程式为二氧化硫被高锰酸钾溶液氧化为硫酸,反应的离子方程式为:
故答案为:品红溶液,澄清石灰水;5SO2+2H2O+2MnO4-=5SO42-+2Mn2++4H+;
点评 本题考查了浓硫酸的性质,题目难度中等,试题侧重基础知识的考查,注意掌握的浓硫酸的三大性质:强酸性、强氧化性和脱水性,能够正确书写常见反应的化学方程式.


科目:高中化学 来源: 题型:选择题
| A. | 只含共价键的物质一定是共价化合物 | |
| B. | HF、HCl、HBr、HI沸点逐渐增加是因为分子量逐渐增加 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 金属与非金属之间形成的是离子键,非金属之间则形成的是共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结构示意图为 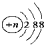 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | |
| B. | 球棍模型为  的分子可发生加成反应 的分子可发生加成反应 | |
| C. | 邻硝基甲苯的结构简式为 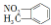 ,能发生取代反应 ,能发生取代反应 | |
| D. | 电子式分别为  和 和 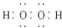 的两种化合物均为常见的氧化剂 的两种化合物均为常见的氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
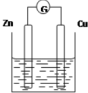 如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 组成该晶体的微粒为分子 | |
| B. | 1mol该晶体中有2mol共价键 | |
| C. | 该二氧化碳晶体和干冰存在的作用力完全相同 | |
| D. | 一定条件下该晶体能与氢氧化钠反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com