
ΓΨΧβΡΩΓΩ»βΙπΥα «œψΝœΓΔΜ·Ή±ΤΖΓΔ“Ϋ“©ΓΔΥήΝœΚΆΗ–Ιβ ς÷§Β»ΒΡ÷Ί“Σ‘≠ΝœΘ° Β―ι “”Οœ¬Ν–Ζ¥”Π÷Τ»Γ»βΙπΥαΘ°
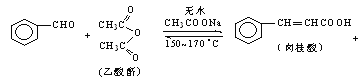 CH3COOH
CH3COOH
“©ΤΖΈοάμ≥Θ ΐ
±ΫΦΉ»© | ““Υατϊ | »βΙπΥα | ““Υα | |
»ήΫβΕ»Θ®25ΓφΘ§g/100gΥ°Θ© | 0.3 | ”ω»»Υ°Υ°Ϋβ | 0.04 | ΜΞ»ή |
Ζ–ΒψΘ®ΓφΘ© | 179.6 | 138.6 | 300 | 118 |
ΧνΩ’ΘΚ
Κœ≥…ΘΚΖ¥”ΠΉΑ÷Ο»γΆΦΥυ ΨΘ°œρ»ΐΨ±…’ΤΩ÷–œ»ΚσΦ”»κ―–œΗΒΡΈόΥ°¥ΉΥαΡΤΓΔ±ΫΦΉ»©ΚΆ““ΥατϊΘ§’ώΒ¥ Ι÷°ΜλΚœΨυ‘»Θ° ‘Ύ150ΓΪ170ΓφΦ”»»1–Γ ±Θ§±Θ≥÷ΈΔΖ–Ή¥Χ§Θ°
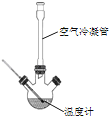
Θ®1Θ©Ω’ΤχάδΡΐΙήΒΡΉς”Ο «__Θ°
Θ®2Θ©ΗΟΉΑ÷ΟΒΡΦ”»»ΖΫΖ® «__Θ°Φ”»»ΜΊΝς“ΣΩΊ÷ΤΖ¥”Π≥ ΈΔΖ–Ή¥Χ§Θ§»γΙϊΨγΝ“Ζ–ΧΎΘ§ΜαΒΦ÷¬»βΙπΥα≤ζ¬ ΫΒΒΆΘ§Ω…ΡήΒΡ‘≠“ρ «______Θ°
Θ®3Θ©≤ΜΡή”Ο¥ΉΥαΡΤΨßΧεΘ®CH3COONa3H2OΘ©ΒΡ‘≠“ρ «______Θ°
¥÷ΤΖΨΪ÷ΤΘΚΫΪ…œ ωΖ¥”ΠΚσΒΟΒΫΒΡΜλΚœΈο≥Ο»»ΒΙ»κ‘≤ΒΉ…’ΤΩ÷–Θ§Ϋχ––œ¬Ν–≤ΌΉςΘΚ
Ζ¥”ΠΜλΚœΈο![]()
![]()
![]()
![]()
![]() »βΙπΥαΨßΧε
»βΙπΥαΨßΧε
Θ®4Θ©Φ”±ΞΚΆNa2CO3»ή“Κ≥ΐΝΥΉΣΜ·¥ΉΥαΘ§÷ς“ΣΡΩΒΡ «_______Θ°
Θ®5Θ©≤ΌΉςI «__ΘΜ»τΥυΒΟ»βΙπΥαΨßΧε÷–»‘»Μ”–‘”÷ Θ§”ϊΧαΗΏ¥ΩΕ»Ω…“‘Ϋχ––ΒΡ≤ΌΉς «__Θ®ΨυΧν≤ΌΉςΟϊ≥ΤΘ©Θ°
Θ®6Θ©…ηΦΤ Β―ιΖΫΑΗΦλ―ι≤ζΤΖ÷– «ΖώΚ§”–±ΫΦΉ»©_______Θ°
ΓΨ¥πΑΗΓΩ ΙΖ¥”ΠΈοάδΡΐΜΊΝς Ω’Τχ‘ΓΘ®Μρ”Ά‘ΓΘ© ““Υατϊ’τ≥ωΘ§Ζ¥”ΠΈοΦθ…ΌΘ§ΤΫΚβΉσ“Τ ““Υατϊ”ω»»Υ°Υ°Ϋβ ΫΪ»βΙπΥαΉΣΜ·ΈΣ»βΙπΥαΡΤΘ§»ήΫβ”ΎΥ° ά以ΫαΨß ÷ΊΫαΨß »Γ―υΘ§Φ”»κ“χΑ±»ή“ΚΙ≤»»Θ§»τ”–“χΨΒ≥ωœ÷Θ§ΥΒΟςΚ§”–±ΫΦΉ»©Θ§ΜρΦ”»κ”Ο–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΘ§»τ≥ωœ÷Ή©Κλ…Ϊ≥ΝΒμΘ§ΥΒΟςΚ§”–±ΫΦΉ»©Θ°
ΓΨΫβΈωΓΩ
(1)ΗυΨί±μ÷–ΗςΈο÷ ΒΡΖ–ΒψΖ÷ΈωΫβ¥πΘΜ
(2)ΗυΨίΖ¥”ΠΧθΦΰΈΣ150ΓΪ170ΓφΘ§―Γ‘ώΦ”»»ΖΫΖ®ΘΜΗυΨί±μ÷–ΗςΈο÷ ΒΡΖ–ΒψΫαΚœΖ¥”ΠΒΡΖΫ≥Χ ΫΖ÷ΈωΫβ¥πΘΜ
(3)ΗυΨί““Υατϊ”ω»»Υ°Υ°ΫβΖ÷ΈωΫβ¥πΘΜ
(4)ΗυΨί»βΙπΥαΡ―»ή”ΎΥ°Θ§Εχ»βΙπΥαΡΤ“Ή»ή”ΎΥ°Ζ÷ΈωΫβ¥πΘΜ
(5)ΗυΨί Ι»βΙπΥα¥”»ή“Κ÷–Έω≥ω“ΜΑψΖΫΖ®ΚΆΈο÷ ΒΡΖ÷άκΧα¥ΩΒΡΖΫΖ®Ζ÷ΈωΫβ¥πΘΜ
(6)Φλ―ι≤ζΤΖ÷– «ΖώΚ§”–±ΫΦΉ»©Θ§Ω…“‘Ά®ΙΐΦ”»κ“χΑ±»ή“ΚΜρ–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΒΡΖΫΖ®Φλ―ιΓΘ
(1)ΗΟΖ¥”Π‘Ύ150ΓΪ170ΓφΒΡΧθΦΰœ¬Ϋχ––Θ§ΗυΨί±μ÷–ΗςΈο÷ ΒΡΖ–ΒψΩ…÷ΣΘ§Ζ¥”ΠΈο‘ΎΗΟΧθΦΰœ¬“ΉΜ”ΖΔΘ§Υυ“‘Ω’ΤχάδΡΐΙήΒΡΉς”Ο « ΙΖ¥”ΠΈοάδΡΐΜΊΝςΘ§ΧαΗΏΖ¥”ΠΈοΒΡάϊ”Ο¬ Θ§Ι ¥πΑΗΈΣΘΚ ΙΖ¥”ΠΈοάδΡΐΜΊΝςΘΜ
(2)”…”ΎΗΟΖ¥”ΠΒΡΧθΦΰΈΣ150ΓΪ170ΓφΘ§Ω…“‘”ΟΩ’Τχ‘Γ(Μρ”Ά‘Γ)ΩΊ÷ΤΘ§‘Ύ150ΓΪ170Γφ ±““Υατϊ“ΉΜ”ΖΔΘ§»γΙϊΨγΝ“Ζ–ΧΎΘ§““Υατϊ’τ≥ωΘ§Ζ¥”ΠΈοΦθ…ΌΘ§ΤΫΚβΡφœρ“ΤΕ·Θ§»βΙπΥα≤ζ¬ ΫΒΒΆΘ§Ι ¥πΑΗΈΣΘΚΩ’Τχ‘Γ(Μρ”Ά‘Γ)ΘΜ““Υατϊ’τ≥ωΘ§Ζ¥”ΠΈοΦθ…ΌΘ§ΤΫΚβΉσ“ΤΘΜ
(3)““Υατϊ”ω»»Υ°“ΉΥ°ΫβΘ§Υυ“‘Ζ¥”Π÷–≤ΜΡή”–Υ°Θ§¥ΉΥαΡΤΨßΧε(CH3COONa3H2O)≤ΈΦ”Ζ¥”ΠΜα”–Υ°Θ§ Ι““ΥατϊΥ°ΫβΘ§Ι ¥πΑΗΈΣΘΚ““Υατϊ”ω»»Υ°Υ°ΫβΘΜ
(4)ΗυΨί±μΗώ ΐΨίΘ§»βΙπΥαΡ―»ή”ΎΥ°Θ§Εχ»βΙπΥαΡΤ“Ή»ή”ΎΥ°Θ§Φ”»κ±ΞΚΆNa2CO3»ή“ΚΩ…“‘ΫΪ»βΙπΥαΉΣΜ·ΈΣ»βΙπΥαΡΤΘ§»ήΫβ”ΎΥ°Θ§±ψ”ΎΈο÷ ΒΡΖ÷άκΧα¥ΩΘ§Ι ¥πΑΗΈΣΘΚΫΪ»βΙπΥαΉΣΜ·ΈΣ»βΙπΥαΡΤΘ§»ήΫβ”ΎΥ°ΘΜ
(5)ΗυΨίΝς≥ΧΆΦΘ§“Σ Ι»βΙπΥα¥”»ή“Κ÷–≥δΖ÷Έω≥ωΘ§“Σά以ΫαΨßΘ§Ι ≤ΌΉςΔώΈΣά以ΫαΨßΘ§ΧαΗΏ»βΙπΥαΒΡ¥ΩΕ»Ω…“‘Ϋχ––÷ΊΫαΨßΘ§Ι ¥πΑΗΈΣΘΚά以ΫαΨßΘΜ÷ΊΫαΨßΘΜ
(6)±ΫΦΉ»©÷–”–»©ΜυΘ§Φλ―ι≤ζΤΖ÷– «ΖώΚ§”–±ΫΦΉ»©Θ§Ω…“‘Ά®ΙΐΦ”»κ“χΑ±»ή“ΚΜρ–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΒΡΖΫΖ®Φλ―ιΘ§≤ΌΉςΈΣΘΚ»Γ―υΘ§Φ”»κ“χΑ±»ή“ΚΙ≤»»Θ§»τ”–“χΨΒ≥ωœ÷Θ§ΥΒΟςΚ§”–±ΫΦΉ»©(ΜρΦ”»κ”Ο–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΘ§»τ≥ωœ÷Ή©Κλ…Ϊ≥ΝΒμΘ§ΥΒΟςΚ§”–±ΫΦΉ»©)Θ§Ι ¥πΑΗΈΣΘΚ»Γ―υΘ§Φ”»κ“χΑ±»ή“ΚΙ≤»»Θ§»τ”–“χΨΒ≥ωœ÷Θ§ΥΒΟςΚ§”–±ΫΦΉ»©(ΜρΦ”»κ”Ο–¬÷Τ«β―θΜ·Ά≠–ϋΉ«“ΚΘ§»τ≥ωœ÷Ή©Κλ…Ϊ≥ΝΒμΘ§ΥΒΟςΚ§”–±ΫΦΉ»©)ΓΘ


 Οϊ–ΘΆ®––÷Λ”––ßΉς“ΒœΒΝ–¥πΑΗ
Οϊ–ΘΆ®––÷Λ”––ßΉς“ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣAG=lg![]() Θ§ΒγάκΕ»ΠΝ=
Θ§ΒγάκΕ»ΠΝ=![]() ΓΝ100%ΓΘ≥ΘΈ¬œ¬Θ§œρ10mL0.1mol/LHX»ή“Κ÷–ΒΈΦ”0.1mol/LNaOH»ή“ΚΘ§ΜλΚœ»ή“Κ÷–AG”κΒΈΦ”NaOH»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΓΘ
ΓΝ100%ΓΘ≥ΘΈ¬œ¬Θ§œρ10mL0.1mol/LHX»ή“Κ÷–ΒΈΦ”0.1mol/LNaOH»ή“ΚΘ§ΜλΚœ»ή“Κ÷–AG”κΒΈΦ”NaOH»ή“ΚΧεΜΐΒΡΙΊœΒ»γΆΦΥυ ΨΓΘ
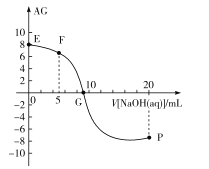
œ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
A.FΒψ»ή“ΚpH<7
B.GΒψ»ή“Κ÷–c(Na+)=cΘ®X-Θ©>c(H+)=cΘ®OH-Θ©
C.V=10 ±Θ§»ή“Κ÷–cΘ®OH-Θ©<c(HX)
D.≥ΘΈ¬œ¬Θ§HXΒΡΒγάκΕ»‘ΦΈΣ1%
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Έ¬Ε»œ¬Θ§œρ10 mL 0.1 mol/LCuCl2»ή“Κ÷–ΒΈΦ”0.1 mol/LΒΡNa2S»ή“ΚΘ§ΒΈΦ”Ιΐ≥Χ÷–»ή“Κ÷–lgc(Cu2+)”κNa2S»ή“ΚΧεΜΐ(V)ΒΡΙΊœΒ»γΆΦΥυ ΨΘ§œ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «

“―÷ΣΘΚlg2ΘΫ0.3Θ§Ksp(ZnS)=3ΓΝ10-25 mol2/L2ΓΘ
A. aΓΔbΓΔc»ΐΒψ÷–Θ§Υ°ΒΡΒγάκ≥ΧΕ»Ήν¥σΒΡΈΣbΒψ
B. Na2S»ή“Κ÷–ΘΚc(H+)+c(HS-)+c(H2S)= c(OH-)
C. ΗΟΈ¬Ε»œ¬Ksp(CuS)=4ΓΝ10-36 mol2/L2
D. œρ100 mL Zn2+ΓΔCu2+≈®Ε»ΨυΈΣ10-5 molL-1ΒΡΜλΚœ»ή“Κ÷–÷πΒΈΦ”»κ10-4 molL-1ΒΡNa2S»ή“ΚΘ§Zn2+œ»≥ΝΒμ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩpH=aΒΡΡ≥ΒγΫβ÷ »ή“Κ÷–Θ§≤ε»κΝΫ÷ßΕη–‘ΒγΦΪΘ§Ά®÷±ΝςΒγ“ΜΕΈ ±ΦδΚσΘ§»ή“ΚΒΡpHΘΨaΘ§‘ρΗΟΒγΫβ÷ Ω…Ρή «
A. Na2SO4 B. H2SO4 C. AgNO3 D. NaCl
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬ΆΦΝΫΗωΉΑ÷Ο÷–Θ§“ΚΧεΧεΜΐΨυΈΣ200mlΘ§ΩΣ Φ ±ΒγΫβ÷ »ή“ΚΒΡ≈®Ε»ΨυΈΣ 0.1mol/LΘ§ΙΛΉς“ΜΕΈ ±ΦδΚσΘ§≤βΒΟΒΦœΏ…œΕΦΆ®ΙΐΝΥ0.02molΒγΉ”Θ§»τ≤ΜΩΦ¬«»ή“ΚΧεΜΐΒΡ±δΜ·Θ§œ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©

A. ≤ζ…ζΤχΧεΧεΜΐΔΌΘΫΔΎ
B. ΒγΦΪ…œΈω≥ωΙΧΧε÷ ΝΩΔΌΘΦΔΎ
C. »ή“ΚΒΡpH±δΜ·ΘΚΔΌΦθ–ΓΔΎ‘ω¥σ
D. ΒγΦΪΖ¥”Π ΫΘΚΔΌ÷–―τΦΪCu2+ΘΪ2eΘ≠ΘΫCuΘ§ΔΎ÷–ΗΚΦΪZnΘ≠2eΘ≠ΘΫZn2+
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΕ®Έ¬Ε»ΖΕΈßΡΎ”Ο¬»Μ·ΡΤ»έΫΰΦΊ≥Λ ·(÷ς“Σ≥…ΖίΈΣKAlSi3O8)Ω…÷ΤΒΟ¬»Μ·ΦΊΘ§÷ς“ΣΖ¥”Π «ΘΚNaCl(l)+KAlSi3O8(s)![]() KCl(l)+NaAlSi3O8(s) ΓςH=-Q kJ/molΓΘ
KCl(l)+NaAlSi3O8(s) ΓςH=-Q kJ/molΓΘ
(1)–¥≥ωCl‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ Ϋ_______Θ§ NaClΒΡ»έΒψ±»KCl______ (―ΓΧνΓΑΗΏΓ±ΜρΓΑΒΆΓ±)ΓΘ
(2)÷Η≥ωΦΊ≥Λ ·÷–¥φ‘ΎΒΡΜ·―ßΦϋάύ–Ά__________________ΓΘ
(3)…œ ωΖ¥”Π…φΦΑΒΡΈΜ”ΎΆ§“Μ÷ήΤΎΒΡΦΗ÷÷‘ΣΥΊ÷–Θ§”–“Μ÷÷‘ΣΥΊΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΚΆΤδ”ύ‘ΣΥΊΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΨυΡήΖΔ…ζΖ¥”ΠΘ§ΗΟ‘ΣΥΊ «_______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦ «÷Τ»ΓΚΆ ’Φ·Ρ≥ΤχΧεΒΡ Β―ιΉΑ÷ΟΘ§ΗΟΉΑ÷ΟΩ…”Ο”Ύ
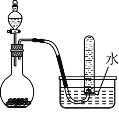
A.”Ο≈®―ΈΥαΚΆΕΰ―θΜ·ΟΧΖ¥”Π÷Τ»ΓCl2
B.”Ο≈®Α±Υ°ΚΆ…ζ ·Μ“Ζ¥”Π÷Τ»ΓNH3
C.”Ο≈®œθΥα”κΆ≠Ζ¥”Π÷Τ»ΓNO2
D.”ΟΙΐ―θΜ·ΡΤΙΧΧεΚΆΥ°Ζ¥”Π÷Τ»ΓO2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœρ13.6g CuΚΆCu2OΒΡΜλΚœΈο÷–Φ”»κΡ≥≈®Ε»ΒΡœΓœθΥα0.25 LΘ§ΙΧΧεΈο÷ Άξ»ΪΖ¥”ΠΘ§…ζ≥…NOΚΆCu(NO3)2ΓΘ‘ΎΥυΒΟ»ή“Κ÷–Φ”»κ0.5 mol/LΒΡNaOH»ή“Κ1 LΘ§Ζ¥”ΠΚσ»ή“Κ«ΓΚΟ≥ ÷––‘Θ§Ϋπ τάκΉ”“―Άξ»Ϊ≥ΝΒμΘ§≥ΝΒμ÷ ΝΩΈΣ19.6 gΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A.Cu”κCu2OΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ2ΓΟ1
B.œθΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ2 mol/L
C.CuΓΔCu2O”κœθΥαΖ¥”ΠΚσ Θ”ύHNO3ΒΡΈο÷ ΒΡΝΩΈΣ0.5 mol
D.≤ζ…ζΒΡNO‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ2.24 L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ–≈œΔ…Η―ΓΘΚ
Δώ.Ρ≥Κ§Ρχ(NiO)ΖœΝœ÷–”–FeOΓΔAl2O3ΓΔMgOΓΔSiO2Β»‘”÷ Θ§”Ο¥ΥΖœΝœΧα»ΓNiSO4ΒΡΙΛ“’Νς≥Χ»γΆΦ1Υυ ΨΘΚ
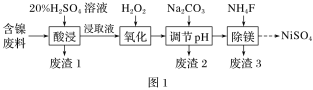
“―÷ΣΘΚΔΌSiO2≤Μ»ή”ΎœΓΝρΥαΓΘ
ΔΎKsp(MgF2)ΘΫ7.4ΓΝ10Θ≠11ΓΘ
Δέ”–ΙΊΫπ τάκΉ”…ζ≥…«β―θΜ·Έο≥ΝΒμΥυ–ηΒΡpH»γΆΦ2Υυ ΨΓΘ
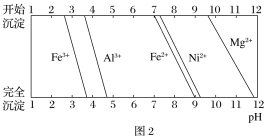
(1)Φ”Na2CO3ΒςΫΎ»ή“ΚΒΡpH÷Ν5Θ§ΒΟΒΫΖœ‘ϋ2ΒΡ÷ς“Σ≥…Ζ÷ «_______________(ΧνΜ·―ß Ϋ)ΓΘ
(2)MgΡή”κ±ΞΚΆNH4Cl»ή“ΚΖ¥”Π≤ζ…ζNH3Θ§«κ”ΟΜ·―ßΤΫΚβ“ΤΕ·‘≠άμΦ”“‘Ϋβ ΆΘΚ___(”Ο±Ί“ΣΒΡΈΡΉ÷ΚΆάκΉ”ΖΫ≥Χ ΫΜΊ¥π)ΓΘ
(3)“―÷Σ≥ΝΒμ«Α»ή“Κ÷–c(Mg2ΘΪ)ΘΫ1.85ΓΝ10Θ≠3 molΓΛLΘ≠1Θ§Β±≥ΐΟΨ¬ ¥οΒΫ99% ±Θ§»ή“Κ÷–c(FΘ≠)ΘΫ_________molΓΛLΘ≠1ΓΘ
(4)‘ΎNaOH»ή“Κ÷–”ΟNaClO”κNiSO4Ζ¥”ΠΩ…÷ΤΒΟNiO(OH)Θ§Μ·―ßΖΫ≥Χ ΫΈΣ______ΓΘ
ΔρΘ°ΒΈΕ®Ζ® «“Μ÷÷÷Ί“ΣΒΡΕ®ΝΩΖ÷ΈωΖΫΖ®Θ§”Π”ΟΖΕΈßΚήΙψΓΘ Β―ι “Ω…Ά®ΙΐΒΈΕ®ΒΡΖΫΖ®≤βΕ®Υυ÷ΤœθΥα“χ―υΤΖΒΡ¥ΩΕ»(‘”÷ ≤Μ≤Έ”κΖ¥”Π)Θ§≤βΕ®Ιΐ≥Χ»γœ¬Θ§“―÷ΣΘΚAgΘΪΘΪSCNΘ≠=AgSCNΓΐ(ΑΉ…Ϊ)ΓΘ
(1)≥Τ»Γ2.000g÷Τ±ΗΒΡœθΥα“χ―υΤΖΘ§Φ”Υ°»ήΫβΘ§Ε®»ίΒΫ100mLΓΘ»ή“Κ≈δ÷ΤΙΐ≥Χ ÷–Υυ”ΟΒΡ≤ΘΝß“«Τς≥ΐ…’±≠ΓΔ≤ΘΝßΑτΆβΜΙ”–_____________________________ΓΘ
(2)ΉΦ»ΖΝΩ»Γ25.00mL»ή“ΚΘ§ΥαΜ·ΚσΒΈ»κΦΗΒΈΧζοßΖΑ[NH4Fe(SO4)2]»ή“ΚΉς÷Η ΨΦΝΘ§‘Ό”Ο0.100molΓΛLΘ≠1NH4SCN±ξΉΦ»ή“ΚΒΈΕ®ΓΘΒΈΕ®÷’ΒψΒΡ Β―ιœ÷œσΈΣ__________ΓΘ
(3)»τΒΈΕ®«ΑΒΈΕ®ΙήΦβΉλ¥Π”–Τχ≈ίΘ§ΒΈΕ®Ιΐ≥Χ÷–ΗΟΤχ≈ίœϊ ßΘ§‘ρΥυ≤βœθΥα“χΒΡ÷ ΝΩΖ÷ ΐ________(ΧνΓΑΤΪΗΏΓ±ΓΑΤΪΒΆΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com